Прогнозирование энтропии образования органических веществСтатьи / Прогнозирование энтропии образования органических веществСтраница 3
Для соединений, имеющих гетероатомы, необходимо также рассматривать пространственное строение структурных фрагментов, в которые входят эти атомы. Например, аминогруппа вместе с ближайшим углеродным атомом обладает структурой пирамиды, поэтому для группы CNH2 число симметрии внутреннего вращения равно единице.
Итак, с вопросом определения чисел симметрии молекул мы в общих чертах познакомились. Наличие в молекуле осей симметрии внутреннего вращения понижает энтропию вещества. Чтобы ввести поправку на симметрию, необходимо из вращательной энтропии вычесть ![]() , т.е.
, т.е.
![]() . (2.8)
. (2.8)
Иной тип поправок приходится вводить в случае, когда интересующее нас вещество имеет хиральные центры и вследствие этого представлено смесью устойчивых форм вращательных изомеров (возможны и другие ситуации). Поскольку энтропия отражает степень упорядоченности системы, то для смеси изомеров необходимо учитывать энтропию смешения
![]() , (2.9)
, (2.9)
где ni - мольная доля i-того изомера в равновесной смеси. Если все изомеры имеют равную энергию, то ni = 1/n и
![]() . (2.10)
. (2.10)
Следовательно, для бинарной смеси с концентрацией каждого изомера 50% или 0,5 мол. долей имеем ![]() = 5,76 Дж/(моль×К).
= 5,76 Дж/(моль×К).
Количество пространственных изомеров органического соединения может быть весьма значительным и зависит от количества элементов хиральности в молекуле, которыми могут быть [31]:
· асимметрические углеродные атомы, т.е. атомы, у которых все четыре заместителя разные, например, центральный атом углерода в молочной кислоте
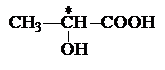 ;
;
· атомы кремния с четырьмя различными заместителями, например, в молекуле метил-(1-нафтил)фенилсилана;
· атомы трехвалентного фосфора в фосфинах или четырехвалентной серы в сульфоксидах с набором различных заместителей при фосфоре или сере, в соединениях которых заместители расположены пирамидально, но структуры являются фактически тетраэдрическими с учетом свободной электронной пары;
· центр молекулы адамантанового ядра с различными заместителями в 1,3,5,7-положениях адамантана;
· оси хиральности, например, для молекул алленов с различными заместителями при крайних углеродных атомах или для 2,2',6,6'-тетра-замещенных бифенилов, размеры заместителей в молекулах которых препятствуют вращению вокруг простой углерод-углеродной связи между ароматическими ядрами, если сумма ван-дер-ваальсовых радиусов орто-заместителей превосходит 0,290 нм; таким соединениям свойственна пространственная изомерия (атропоизомерия - где тропос - поворот (греч.), атропо- нет поворота);
· плоскости хиральности, например, в производных ферроцена;
· спиральность, например, в белках, нуклеиновых кислотах или гелиценах (простейшая модель спиральности) с шестью и более орто-конденсированными бензольными ядрами, которые не могут расположиться в одной плоскости и образуют правую или левую спираль.
Из перечисленных элементов хиральности для относительно несложных структур наиболее часто встречающимися являются асимметрические углеродные атомы. В этом случае максимальное количество оптических изомеров равно ![]() , где “m” - число асимметрических атомов углерода.
, где “m” - число асимметрических атомов углерода.
Если набор заместителей при различных асимметрических углеродных атомах одинаков, то количество оптических изомеров уменьшается вследствие образования мезо-формы. При расчете величины поправки на смешение оптических изомеров в этом случае концентрация мезо-формы в первом приближении может быть принята равной суммарной концентрации равновесной с ней dl-формы. Таким образом, для структур с двумя асимметрическими атомами в молекуле имеем поправку на смешение оптических изомеров, равную
![]() = –8,3147·(0,5·ln(0,5)+0,25·ln(0,25)+0,25·ln(0,25)) =
= –8,3147·(0,5·ln(0,5)+0,25·ln(0,25)+0,25·ln(0,25)) =
= 8,64 Дж/(моль×К).
Если центры асимметрии находятся не при соседних атомах, то весь соединяющий их фрагмент считают за одну связь.
Наличие асимметрических углеродных атомов в циклических соединениях также требует при прогнозировании энтропии учета вклада на смешение оптических изомеров. Однако при этом необходимо учитывать специфику строения молекул интересующего циклического соединения.
