ЖелезоМатериалы / ЖелезоСтраница 1
ПОБОЧНАЯ ПОДГРУППА ВОСЬМОЙ ГРУППЫ
Побочная подгруппа восьмой группы периодической системы охватывает три триады d-элементов. Первую триаду образуют элементы железо, кобальт и никель, вторую триаду — рутений, родий и палладий и третью триаду — осмий, иридий и платина.
На сестру mobixit.ru/ringtony-na-sestru/ рингтоны скачать . Продажа сейфов kazan.profsafe.ru/safes/.Большинство элементов рассматриваемой подгруппы имеют два электрона в наружном электронном слое атома; все они представляют собой металлы. Кроме наружных электронов, в образовании химических связей принимают участие также электроны из предыдущего недостроенного слоя. Для этих элементов характерны степени окисленности, равные 2, 3, 4. Более высокие степени окисленности проявляются реже. В периодической системе железо находится в четвертом периоде, в побочной подгруппе VIII группы.
Химический знак — Fе (феррум). Порядковый номер — 26, электронная формула 1s22s22p63s23p63d64s2. Электронно-графическая формула:
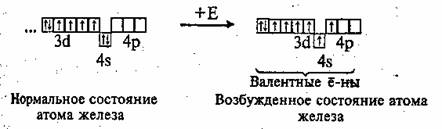
Валентные электроны у атома железа находятся на последнем электронном слое (4s2) и предпоследнем (Зd6). В химических реакциях железо может отдавать эти электроны и проявлять степени окисления +2, +3 и иногда +6.
Сравнение физических и химических свойств элементов восьмой группы показывает, что железо, кобальт и никель, находящиеся в первом большом периоде, очень сходны между собой и в то же время сильно отличаются от элементов двух других триад. Поэтому их обычно выделяют в семейство железа. Остальные шесть элементов восьмой группы объединяются под общим названием платиновых металлов.
СЕМЕЙСТВО ЖЕЛЕЗА
. Железо (Ferrum). Нахождение в природе. Железо—самый распространенный после алюминия металл на земном шаре: оно
Таблица: Некоторые свойства железа, кобальта и никеля
|
Ре |
Со |
N1 | |
|
Радиус атома, нм |
0,126 |
0,125 |
0,124 |
|
Энергия ионизации | |||
|
Э → Э+, эВ |
7,89 |
7,87 |
7,63 |
|
Э+ → Э2+, эВ |
16,2 |
17,1 |
18,15 |
|
Э2+, → ЭЗ+, эВ |
30,6 |
33,5 |
35,16 |
|
Радиус иона Э2+, нм |
0,080 |
0,078 |
0,074 |
|
Радиус иона Э3+, нм |
0,067 |
0,064 | |
|
Стандартная энтальпия ато- |
417,0 |
428,4 |
428,8 |
|
мизации металла при 25° С, | |||
|
кДж на 1 моль атомов | |||
|
Плотность, г/см3 |
7,87 |
8,84 |
8,91 |
|
Температура плавления, °С |
1539 |
1492 |
1455 |
|
Температура кипения, °С |
2870 |
3100 |
2900 |
|
Стандартный электродный по |
-0,440 |
-0,277 |
—0,250 |
|
тенциал процесса Э2 + | |||
|
+2е=Э, В |
Смотрите также
Кислород (Oxygenium), О
Кислород - химический элемент VI группы периодической системы Менделеева; атомный номер 8, атомная масса 15,9994. При нормальных условиях К. - газ без цвета, запаха и вкуса. Трудно назвать другой элем ...
Фосфор (Phosphorus), Р
В темной комнате или ночью на улице попробуйте сделать такой простой опыт. Не очень сильно, так, чтобы не загорелась спичка, чиркните ею по спичечной коробке. Вы заметите, что некоторое время на терке ...
Комплексные соединения
Комплексные
соединения довольно широко распространены в природе. В области химии возник
большой раздел - комплексные соединения. Меня эта тема заинтересовала и поэтому
я решила более подроб ...
