Комплексы. Связи координационная, дативная. Обратное связываниеПериодическая система / Комплексы. Связи координационная, дативная. Обратное связываниеСтраница 4
Полярные связи и МО:
Образуется общая пара, она смещена
Li-H « Li+ H- ¬ либо к атому H
H- F « H + F- ¬ либо от атома H
Представим МО у молекул с полярными связями в следующем виде:
LiH; j(LiH) = h±´1s(H)± l±´2s(H) (-13.6; -5.5) эВ ® h±>l± ® h±2>l±2
HF; j(HF) = h±´1s(H) ± f±´2p(F) (-13.6; -17.4) эВ ® h±<f± ® h±2<f±2
Уровень связывающей МО всегда ниже нижнего уровня исходных АО.
Уровень разрыхлюящей МО всегда выше высшего уровня исходных АО.
Зарядовая асимметрия очень высокая.
Вектор дипольного момента считается направленным от плюса к минусу.
Пиктограммы и профильные диаграммы имеют больший «всплеск» у атома, у которого базисная АО лежит ниже. Он акцептор. К нему смещена электронная плотность. Вектор дипольного момента ориентирован от плюса к минусу.
Эта связь полярная. Она и ковалентная, и частично ионная одновременно, однако без полного переноса электронов от одного атома к другому. Электронное облако деформировано. Есть аналогия со связью донорно-акцепторного типа, но в полярной связи электронная пара совместная – по одному электрону от каждого атома, образующего связь, и резонансные структуры учитывают и пару электронов, и частичное смещение заряда. Полного переноса электронов от одного атома к другому нет.
Полярная связь описывается наложением раздельных ковалентной и ионной структур.
m (LiH)= -5.9 D Li+ H- « Li¾H
m (HF) = 1.8 D H+ F- « H ¾F
Напротив, у донорно-акцепторной связи этих символы пишутся раздельно.
Химические символы всегда беднее оригинала. Электронно-ядерная структура молекулы сложнее, чем могут передать графические средства и символы, выработанные современной теорией.
В органической химии для качественного изображения электронного распределения на полярной связи используют один из графических способов посредством изогнутых стрелок, указывающих смещение зарядов.
Получить числа – коэффициенты при базисных АО в составе МО легко прямым расчётом МО ЛКАО как в упрощённых версиях теории, так и в неэмпирических расчётах.
Полярная связь является одним из наиболее распространённых видов связи .
В сочетании с ионной связью и донорно-акцепторными взаимодействиями можно качественно описать множество известных молекулярных структур
Типы химических связей (простое перечисление):
1) Гомеополярная (ковалентная)
2) Гетерополярная (ионная)
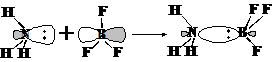

3) Полярная (валентные символы)
4) Донорно-акцепторная (валентные символы)
5) Металлическая
6) Водородная
7) Силы Ван-дер-Ваальса
Орбитальные характеристики атомов 1-2 Периодов.
По теореме Купманса потенциалы ионизации суть энергии орбиталей с обратным знаком. В таблице приведены потенциалы ионизации и электронное сродство.
|
H |
Li |
Be |
B |
C |
N |
O |
F |
Ne | |
|
Z |
1 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
1-й ПИ, эВ |
13.62 |
5.377 |
9.281 |
8.28 |
11.23 |
14.48 |
13.57 |
17.37 |
21.509 |
|
ЭС, эВ |
0.747 |
0.82 |
-0.19 |
0.38 |
2.1;1.12 |
0.05 |
1.465 |
3.58;3.50 |
- |
|
DE2s2p, эВ |
теор. |
1.85 |
3.36 |
5.76 |
8.77 |
12.39 |
16.53 |
21.54 |
Смотрите также
Ксенон (Xenonum), Xe
Ксенон - химический элемент VIII группы периодической системы Д. И. Менделеева, относится к инертным газам; ат. н. 54, ат. м. 131,30. На Земле К. присутствует главным образом в атмосфере. Атмосферный ...
Барий (Baryum), Ba
Защитные стенки рентгеновских установок медицинского и научного назначения делают из кирпича, содержащего соединения бария. Прекрасный поглотитель рентгеновских лучей - барий применяется исключительно ...
Устранение слабых сторон заводского технологического процесса, а также снижения трудоемкости и себестоимости технологического процесса механической обработки путем перевода технологического процесса
Объем работы – 108
листов, имеются иллюстрации и таблицы.
Графическая часть
содержит 10 листов формата А1, в качестве приложений приведены спецификации на
разработанные нами приспособлен ...
