Теория структурообразованияСтатьи / Теория структурообразованияСтраница 3
При n = 1 жидкость ньютоновская (кривая 1 рис. 4.1.2.1). Отклонение n от 1 характеризует степень отклонения свойств жидкости от ньютоновских.
Разбавленные дисперсные системы с равноосными частицами обычно – ньютоновские жидкости. Псевдопластические жидкости – суспензии с асимметричными частицами, растворы полимеров производные целлюлозы). Дилатантные жидкости в химической технологии встречаются редко, их свойствыа характерны для некоторых керамических масс. Дилатантное поведение наблюдается у дисперсных систем с большим содержанием твердой фазы.
Теория быстрой коагуляции, разработанная М. Смолуховским в 1916 г., основана на следующих положениях.
1. Рассматриваемая система является монодисперсной, радиус частиц r.
2. ![]() , т.е. все столкновения являются эффективными.
, т.е. все столкновения являются эффективными.
3. Рассматриваются только столкновения первичных частиц.
4. Кинетика коагуляции подобна кинетике бимолекулярной реакции:
![]() ,
,
где k – константа скорости коагуляции.
Проинтегрируем это уравнение, разделив переменные:
![]()
![]() ,
,
где u0 – концентрация частиц золя в начальный момент времени;
ut – концентрация частиц золя в момент времени t.
Для характеристики быстрой коагуляции используется период коагуляции(период половинной коагуляции) q.
Период коагуляции (
q
) – это время, через которое концентрация коллоидных частиц уменьшается в два раза
.
При ![]()
![]()
Согласно теории быстрой коагуляции, константа коагуляции зависит от коэффициента диффузии и может быть вычислена по уравнению
![]()
Если подставить в это уравнение величину коэффициента диффузии, получим:
![]()
Таким образом, зная вязкость дисперсионной среды и температуру, можно вычислить константу скорости быстрой коагуляции. Теория Смолуховского неоднократно проверялась экспериментально и получила блестящее подтверждение, несмотря на сделанные автором допущения.
Медленная коагуляция связана с неполной эффективностью столкновений вследствие существования энергетического барьера. Простое введение величины степени коагуляции a в формулы теории Смолуховского не привело к согласию теории с опытом. Более совершенную теорию медленной коагуляции разработал Н.Фукс. Он ввел в кинетическое уравнение коагуляции множитель, учитывающий энергетический барьер коагуляции ΔU к:
![]() ,
,
где kКМ – константа скорости медленной коагуляции;
kКБ - константа скорости быстрой коагуляции;
Р – стерический фактор;
ΔUк - потенциальный барьер коагуляции;
k – постоянная Больцмана.
Таким образом, для расчета константы скорости медленной коагуляции необходимо знать потенциальный барьер коагуляции, величина которого зависит прежде всего от z– потенциала.
Фактор устойчивости
, или коэффициент замедления W, показывает, во сколько раз константа скорости медленной коагуляции меньше константы скорости быстрой коагуляции.
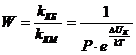 ,
,
Следует отметить пять факторов устойчивости, среди которых два первых играют главную роль.
1. Электростатический фактор устойчивости.
Он обусловлен наличием ДЭС и x– потенциала на поверхности частиц дисперсной фазы.
2. Адсорбционно – сольватный фактор устойчивости.
Он обусловлен снижением поверхностного натяжения в результате взаимодействия дисперсионной среды с частицей дисперсной фазы. Этот фактор играет заметную роль, когда в качестве стабилизаторов используются коллоидные ПАВ.
3. Структурно – механический фактор устойчивости.
Он обусловлен тем, что на поверхности частиц дисперсной фазы образуются пленки, обладающие упругостью и механической прочностью, разрушение которых требует времени и затраты энергии. Этот фактор устойчивости реализуется в тех случаях, когда в качестве стабилизаторов используются высокомолекулярные соединения (ВМС).
4. Энтропийный фактор устойчивости.
Коагуляция приводит к уменьшению числа частиц в системе, следовательно, к уменьшению энтропии (ΔS<0), а это приводит к увеличению свободной энергии системы ΔG>0. Поэтому система самопроизвольно стремится оттолкнуть частицы друг от друга и равномерно (хаотично) распределить по объему системы. Этим обусловлен энтропийный фактор устойчивости. Однако число частиц в коллоидном растворе по сравнению с истинным раствором такой же массовой концентрации гораздо меньше, поэтому роль энтропийного фактора невелика. Но если частицы стабилизированы веществами, обладающими длинными гибкими цепями (ВМС) и потому имеющими много конформаций, то при сближении таких частиц их защитные слои вступают во взаимодействие. Это взаимодействие непременно приводит к уменьшению числа возможных конформаций, а значит – к уменьшению энтропии. Поэтому система стремится оттолкнуть частицы друг от друга.
Смотрите также
Исследования Николая Зинина
Николай
Зинин родился 13 (25) августа 1812, г. Шуша Елизаветпольской губернии,
ныне в Нагорном Карабахе. Скончался 6 (18) февраля 1880, в Петербурге.
...
Химические соединения на основе кремния и углерода
Химия - одна из
отраслей естествознания, предметом изучения которой являются химические
элементы (атомы), образуемые ими простые и сложные вещества (молекулы), их
превращения и законы, кото ...
Методика определения массовой доли парафина
Методика
определения массовой доли парафина
по
ГОСТ 11851-85. (метод А)
Сущность метода А заключается в предварительном
удалении асфальтово-смолистых веществ из нефти, их э ...
