Правила, механизм и кинетика коагуляцииСтатьи / Правила, механизм и кинетика коагуляцииСтраница 3
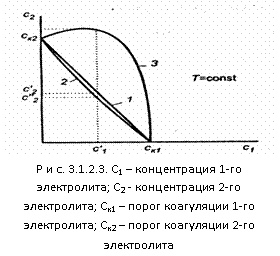
При коагуляции золя смесью двух и более электролитов возможны три случая (рис. 3.1.2.3). По оси абсцисс отложена концентрация первого электролита С1, а Cк1 – его порог коагуляции. Аналогично по оси ординат отложена концентрация второго электролита С2, а Ск2 – его порог коагуляции.
1. Аддитивное действие электролитов (линия 1 рис. 3.1.2.3). Электролиты действуют как бы независимо один от другого, их суммарное действие складывается из воздействий каждого из электролитов. Если с1´ - концентрация первого электролита, то для коагуляции золя концентрация второго электролита должна быть равной с2´. Аддитивность наблюдается обычно при сходстве коагулирующей способности обоих электролитов.
2. Синергизм действия (линия 2 рис. 3.1.2.3). Электролиты как бы способствуют друг другу – для коагуляции их требуется меньше, чем нужно по правилу аддитивности (с2″ < c2′). Условия, при которых наблюдается синергизм, сформулировать трудно.
3. Антагонизм действия (линия 3 рис. 3.1.2.3). Электролиты как бы противодействуют друг другу и для коагуляции их следует добавить больше, чем требуется по правилу аддитивности. Антагонизм наблюдается при большом различии в коагулирующем действии электролитов.
Существует несколько теорий, объясняющих явление антагонизма. Одной из его причин может служить химическое взаимодействие между ионами.
Например, для золя AgCl, стабилизированного хлоридом калия, коагулирующем действием обладают катионы. Например, большой коагулирующей способностью обладает четырёхзарядный ион тория Th4+. Однако если взять для коагуляции смесь Th(NO3)4 и K2SO4, то коагулирующая способность этой смеси значительно меньше, чем отдельно взятого Th(NO3)4. Связано это с тем, что в результате химической реакции образуется комплекс:
![]()
и вместо четырёхзарядных ионов Th4+ в золе будут находиться однозарядные катионы K+, коагулирующее действие которых значительно слабее (правило Шульце-Гарди).
Гетероадагуляция- прилипание частиц дисперсной фазы к вводимой в систему чужеродной поверхности.
Одной из причин этого явления является адсорбция стабилизатора на этой поверхности. Например: отложение коллоидных частиц на волокнах при крашении и дроблении.
Для гидрофобных золей в качестве ВМС обычно используют белки, углеводы, пектины; для неводных золей – каучуки.
При введении в коллоидный раствор электролитов, содержащих многовалентные ионы с зарядом противоположные заряду частиц, наблюдается явление "неправильные ряды". Оно состоит в том, что при добавлении к отдельным порциям золя все возрастающего его количества электролита золь сначала остается устойчивым, затем в определенном интервале концентраций происходит коагуляция; далее золь снова становится устойчивым и, наконец, при повышении концентрации электролита опять наступает коагуляция уже окончательная. Подобные явления могут вызывать и большие органические ионы. Объясняется это тем, что при весьма малых количествах введенного электролита ионов недостаточно, чтобы коагулировать золь, т. е. значение x- потенциала остается выше привычного (рис. 3.1.2.4). При больших количествах электролита его ионы проявляют коагулирующее действие. Этот интервал концентраций отвечает значениям x- потенциала частиц от x критического первого знака до x критического другого знака.

При еще больших концентрациях многовалентные ионы перезаряжают коллоидную частицу и золь опять устойчивый. В этой зоне x-потенциал опять выше критического значения, но обратен по знаку частицам исходного золя. Наконец, при высоком содержании исходного электролита многовалентные ионы снова снижают значение x-потенциала ниже критического и снова происходит окончательная коагуляция.
Повышение агрегативной устойчивости золя путём введения в него высокомолекулярного соединения (ВМС) называется коллоидной защитой. Происходит образование защитной пленки на поверхности золя (гидратной или ВМС), препятствующей взаимодействию частиц электролита.
В качестве количественной характеристики коагуляции Зигмонди предложил использовать скорость коагуляции.
Скорость коагуляции
u
- это изменение концентрации коллоидных частиц в единицу времени при постоянном объеме системы
.
![]() ,
,
Смотрите также
Предмет аналитической химии. История и применение
...
Три теории деформационного учета монокристаллов
Среди многих неясных вопросов в проблеме пластичности монокристаллов
вопрос о природе деформационного упрочнения, которое состоит в увеличении
сопротивляемости кристалла пластической деформ ...
