Правила, механизм и кинетика коагуляцииСтатьи / Правила, механизм и кинетика коагуляцииСтраница 2
Рассмотрим концентрационную коагуляцию золя хлорида серебра, стабилизированного нитратом серебра, при введении в золь нитрата калия.
Формула мицеллы имеет вид:
![]() .
.
На рис. 3.1.2.1 показан график изменения потенциала в ДЭС мицеллы хлорида серебра. Кривая 1 относится к исходной мицелле, кривая 2 – после добавления KNO3 в количестве, вызывающем коагуляцию. При добавлении KNO3 диффузный слой противоионов сжимается, формула мицеллы приобретает вид:
![]()
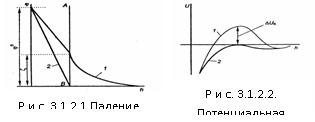
На рис. 3.1.2.2 представлены потенциальные кривые, характеризующие взаимодействие частиц в этом золе. z-потенциал исходной коллоидной частицы положительный, это создаёт потенциальный барьер коагуляции ∆Uк=0 (кривая 2 рис. 3.1.2.2). Поэтому ничто не мешает коллоидным частицам сблизиться на такое расстояние, где преобладают силы притяжения – происходит коагуляция. Так как в данном случае причиной коагуляции является увеличение концентрации противоионов, она называется концентрационной коагуляцией.
Для этого случая теория дает формулу
![]()
где g - порог коагуляции;
С – константа, слабо зависящая от асимметрии электролита, т.е. отношение числа зарядов катиона и аниона;
А – константа;
е – заряд электрона;
e - диэлектрическая проницаемость;
Z – заряд коагулирующего иона;
Т – температура.
Из уравнения следует, что значение порогов коагуляции для одно-, двух-, трех-, четырех- зарядных ионов должны соотноситься 1 к (1/2)6 к (1/3)6 к (1/4)6 и т.д., т.е. обосновывается ранее представленное эмпирическое правило Шульце – Гарди.
Нейтрализационная коагуляция
происходит при добавлении к золю неиндифферентного электролита. При этом потенциалопределяющие ионы связываются в малорастворимое соединение, что приводит к уменьшению абсолютных величин термодинамического потенциала, а следовательно, и z-потенциала вплоть до нуля.
Если взять в качестве исходного только что рассмотренный золь хлорида серебра, то для нейтрализации потенциалопределяющих ионов Ag+ в золь необходимо ввести, например, хлорид калия. После добавления определённого количества этого неиндифферентного электролита мицелла будет иметь вид:
![]()
В системе не будет ионов, способных адсорбироваться на поверхности частицы AgCl, и поверхность станет электронейтральной. При столкновении таких частиц происходит коагуляция.
Так как причиной коагуляции в данном случае является нейтрализация потенциалопределяющих ионов, такую коагуляцию называют нейтрализационной коагуляцией.
Необходимо отметить, что для полной нейтрализационной коагуляции неиндифферентный электролит должен быть добавлен в строго эквивалентном количестве.
При коагуляции смесью электролитов различают два типа процессов:
· гомокоагуляция
· гетерокоагуляция
Гомокоагуляция- укрупнение подобных частиц в больший агрегат осадка. Причем в процессе отстаивания мелкие частицы растворяются, а крупные увеличиваются за их счет. На этом основано явление активации и перекристаллизации. Этот процесс описывается уравнением Кельвина – Томсона:
![]() ,
,
где С¥ - растворимость макрочастиц;
С – растворимость микрочастиц;
Vм – молярный объем;
R – универсальная газовая постоянная;
T – температура;
r – радиус частиц.
Из уравнения следует, что концентрация вокруг маленького радиуса больше, поэтому диффузия идет от бóльшей концентрации к меньшей.
При втором типе происходит слияние разнородных частиц или прилипание частиц дисперсной системы на вводимые в систему чужеродные тела или поверхности.
Гетерокоагуляция- взаимная коагуляция разнородных дисперсных систем.
Коагуляция смесью электролитов имеет большое практическое значение, так как даже при добавлении к золю одного электролита-коагулянта, в действительности коагуляция происходит, по крайней мере, под влиянием двух электролитов, так как в системе содержится электролит-стабилизатор. Кроме того, в технике для коагуляции часто применяют смесь двух электролитов. Понимание закономерностей взаимного действия электролитов важно также при исследовании воздействия биологически активных ионов на органы и ткани живого организма.
Смотрите также
Коллоиды как лекарственные средства.
Столь чужеродно звучащее слово «коллоид» происходит от греческого
слова «коlla» – клей. Коллоиды знакомы нам под другими названиями. Так,
большие молекулы протеинов, полисахаридов и нуклеиновых кисл ...
Моделирование парожидкостного равновесия реакционной смеси в процессе получения
Метилциклопропилкетон (МЦПК) – важный
полупродукт органического синтеза. Одним из способов его получения является
реакция разложения ацетопропилацетата с выделением уксусной кислоты (УК) [1] ...
Технология получения высокоочищенного хитозана из панцирей ракообразных
...
