Химическая кинетика и равновесиеМатериалы / Химическая кинетика и равновесиеСтраница 2
![]() – показатель порядка реакции в целом (реакции первого, второго, третьего … порядков).
– показатель порядка реакции в целом (реакции первого, второго, третьего … порядков).
Число частиц, участвующих в этом акте реакции определяет молекулярность реакции:
![]() мономолекулярная (
мономолекулярная (![]() )
)
![]() бимолекулярная (
бимолекулярная (![]() )
)
![]() тримолекулярная.
тримолекулярная.
Больше 3‑х не бывает, т.к. столкновение более 3‑х частиц сразу – маловероятно.
Когда реакция идёт в несколько стадий, то общая ![]() реакции =
реакции = ![]() наиболее медленной стадии (лимитирующей стадии).
наиболее медленной стадии (лимитирующей стадии).
Зависимость скорости реакции от температуры определяется эмпирическим правилом Вант-Гоффа: при увеличении температуры на ![]() , скорость химической реакции увеличивается в 2 – 4 раза:
, скорость химической реакции увеличивается в 2 – 4 раза: ![]() .
.
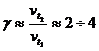
![]() ,
,
где ![]() – температурный коэффициент скорости химической реакции
– температурный коэффициент скорости химической реакции 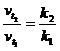 .
.
Не всякое столкновение молекул сопровождается их взаимодействием. Большинство молекул отскакивают как упругие шарики. И только активные при столкновении взаимодействуют друг с другом. Активные молекулы обладают некоторой избыточной ![]() но сравнению с неактивными молекулами, поэтому в активных молекулах связи между ними ослаблены.
но сравнению с неактивными молекулами, поэтому в активных молекулах связи между ними ослаблены.
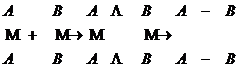
Энергия для перевода молекулы в активное состояние – энергия активации ![]() . Чем она меньше, тем больше частиц реагируют, тем больше скорость химической реакции.
. Чем она меньше, тем больше частиц реагируют, тем больше скорость химической реакции.
Величина ![]() зависит от природы реагирующих веществ. Она меньше
зависит от природы реагирующих веществ. Она меньше ![]() диссоциации – наименее прочной связи в реагентах.
диссоциации – наименее прочной связи в реагентах.
Изменение ![]() в ходе реакции:
в ходе реакции:
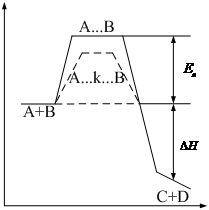
![]() выделяется (экзотермическая)
выделяется (экзотермическая)
С увеличением температуры число активных молекул растёт, поэтому ![]() увеличивается.
увеличивается.
Константа ![]() химической реакции связана с
химической реакции связана с
![]() :
: ![]() ,
,
где ![]() – предэкспоненциальный множитель (связан с вероятностью и числом столкновений).
– предэкспоненциальный множитель (связан с вероятностью и числом столкновений).
В зависимости от природы реагирующих веществ и условий их взаимодействия, в элементарных актах реакций могут принимать участие атомы, молекулы, радикалы или ионы.
Свободные радикалы чрезвычайно реакционноспособны, ![]() активных радикальных реакций очень мала (
активных радикальных реакций очень мала (![]() ).
).
