Теория химико-технологических процессов органического синтезаСтатьи / Теория химико-технологических процессов органического синтезаСтраница 9
По полученным данным рассчитываем термодинамические характеристики процесса:
![]()
![]()
Рассчитаем константу равновесия реакции ![]() при стандартном давлении для диапазона температур:
при стандартном давлении для диапазона температур:
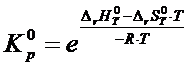 .
.
Результаты расчетов сводим в таблицу:
|
|
| |
|
298 |
158574,80 |
388,41 |
|
400 |
166620,46 |
391,47 |
|
500 |
173295,78 |
390,45 |
|
600 |
179325,50 |
387,84 |
|
800 |
190676,71 |
381,98 |
|
1000 |
201989,69 |
376,59 |
Т. о., можно сделать вывод, что реакция эндотермическая, т.е. при увеличении температуры увеличивается скорость прямой реакции. По уравнению реакции можно сделать вывод, что при увеличении давления реакция разложения диоксана замедлится, т.е. увеличение давления в реакторе нежелательно.
Рассчитаем константу равновесия для различных температур
Кр = exp(-∆G/R*T), где ∆G = ∆Gвода + ∆Gформальд + ∆Gизопрен - ∆Gдмд
|
Т |
∆G |
Кр |
|
298 |
31860,41 |
2,60122E-06 |
|
400 |
-15415,4 |
103,0660931 |
|
500 |
-44317,5 |
42656,70466 |
|
600 |
-100209 |
530048492,7 |
|
800 |
-192507 |
3,71431E+12 |
|
1000 |
-283127 |
6,15968E+14 |
Определим степень конверсии при различных температурах
Х = (-Кр*n + Kp^2*n^2+4*(Kp+Pобщ) *(n+1) *Kp) /(2*Kp+Pобщ)
где n – кол-во молей инертного разбавителя
Pобщ – общее давление
|
T |
X |
|
298 |
0,00032045 |
|
400 |
0,945420958 |
|
500 |
0,999999972 |
|
600 |
1 |
|
800 |
1 |
|
1000 |
1 |
Смотрите также
Методы разделения азеотропных смесей
...
Учёные создали золотой алюминий и синее серебро
Физики из института оптики Университета Рочестера поменяли стандартный серебристый цвет алюминия на золотой, потом на голубой, а затем на серый. Впоследствии оказалось, что не только этот металл спосо ...
