Радикально-цепные процессыПериодическая система / Моделирование газофазных процессов, протекающих при гетерогенно-каталитическом восстановлении оксидов / Радикально-цепные процессы
В литературе существует ряд работ, показывающих, что большинство реальных химических реакций являются сложными и идут через посредство активных промежуточных продуктов. Реакция между двумя стабильными молекулами требует большой энергии активации. Поэтому скорость такой реакции мала. Реально наблюдаемые нами реакции идут обычно "окольными" путями, позволяющими обойти этот высокий энергетический барьер.
В случае гомогенных реакций первой стадией является обычно образование из исходных веществ тех или иных активных промежуточных продуктов. Природа этих продуктов в настоящее время еще недостаточно хорошо изучена, но, надо полагать, она может быть различной. Во многих случаях роль активных промежуточных продуктов, несомненно, играют свободные радикалы или даже свободные атомы. В других случаях это могут быть и довольно сложные и относительно стабильные молекулы, обладающие, однако, по тем или иным причинам, повышенной реакционной способностью, например, органические перекиси.
Активные промежуточные продукты, реагируя с исходными веществами, переводят их в конечные продукты реакции. Эти процессы требуют сравнительно малой энергии активации (особенно когда активными продуктами являются свободные радикалы или атомы) и идут с большей скоростью. Но первичное образование активных продуктов из стабильных исходных молекул требует большой энергии активации, и поэтому с большой скоростью проходить не может.
Для того чтобы реакция посредством активных продуктов могла протекать достаточно быстро, необходимо, чтобы активные продукты регенерировались при реакции, т.е. чтобы при взаимодействии активных продуктов с исходными веществами получались не только стабильные конечные продукты реакции, но и новые молекулы активных промежуточных продуктов. Такие реакции, в которых имеет место регенерация активных промежуточных продуктов, называются цепными(3, стр 17) Как было установлено Семеновым, Хиншельвудом и др., большинство реальных гомогенных сложных реакций являются цепными.
Обозначим концентрацию активного продукта как x. Изменение этой величины со временем для цепных реакций подчиняется следующему кинетическому уравнению:
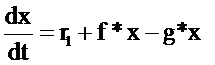
где no – скорость зарождения цепей;
f – константа скорости процесса разветвления цепей (в общем случае не совпадает с общепринятым понятием константы скорости элементарной реакции
g - константа скорости обрыва цепей.
Под зарождением цепей подразумевают начальный процесс образования продукта из исходных веществ, под разветвлением цепей – процесс, в котором одна молекула активного продукта, реагируя с исходными веществами, вызывает образование двух или нескольких молекул активного продукта; под обрывом цепей – процесс, при котором активный продукт безвозвратно уничтожается.
