Приложение 13
Растворенный углекислый газ в воде определяет жизнедеятельность в океане. Углекислый газ является “продуктом питания” фитопланктона. Максимальное содержание углекислого газа приурочено к глубинным слоям воды. Растворимость углекислоты возрастает в холодных водах и уменьшается при нагревании. В связи с этим в зимние месяцы часть углекислого газа переходит из атмосферы в океаническую воду, а летом – обратно.
Углекислый газ принимает участие в химических реакциях, в частности регулирует карбонатное равновесие. Воды, обогащенные углекислым газом, агрессивны по отношению к CaCO3, удаление углекислого газа из воды при ее нагревании способствует осаждению карбонатов. Велика роль углекислого газа в фотосинтезе, в процессе которого образуется органическое вещество. В результате фотосинтеза в океане ежегодно образуется около 1017 г биомассы фитопланктона.
Выяснив, что углекислый газ может поглощать океан как северного, так и южного полушария, ученых заинтересовал еще один вопрос: поглощает ли южная часть Тихого океана углекислый газ во все сезоны года?
Известно, что обильный планктон южного полушария играет важную роль в природном механизме, “выкачивающем” диоксид углерода из атмосферы и отлагающем ее в меловые осадочные породы морского дна. Если его эффективность понизится, количество углекислого газа в воздухе возрастает, что будет способствовать парниковому эффекту, вызывающему глобальное потепление.
На сессии Американского географического союза в декабре 1991 г. были представлены первые материалы о концентрациях углекислого газа в водах южной части Тихого океана в осенний период. Исследования выполняли сотрудники Тихоокеанской лаборатории Национального управления США по изучению океана и атмосферы (НОАА) Р.Фили и П.Мерфи при участии Р.Гаммона – Вашингтонский университет, спонсор исследования – программа НОАА по глобальному изменению климата.
Обобщенные данные непосредственных химических анализов, которые были выполнены с 1984 по 1989 г. в Тихом океане от экватора до Южного полярного круга. Полученные результаты ставят под сомнение представление о роли этой области Мирового океана как активного поглотителя углекислого газа из атмосферы.
На основании прежних исследований считалось, что около половины углекислого газа, поступающего в атмосферу со всей земной поверхности при сжигании ископаемого топлива и сокращении площади лесных массивов, в ней и остается, а другая половина – “пропавший углерод” – поглощается наземными растениями и водами океана, в основном южной частью Тихого океана. Считалось также, что область высоких концентраций углекислого газа в восточной половине южной части Тихого океана находится в приблизительном балансе с областью низких концентраций западной половины.
По мнению Фили, “область высоких концентраций углекислого газа – это те районы, где океан отдает этот газ в атмосферу, и наоборот, в области с низкими концентрациями углекислого газа воды поглощают его из атмосферы”. Однако количество поглощаемой и отдаваемой углекислоты зависит от скорости ветра: чем он сильнее, тем больше углекислого газа переносится через границу вода-воздух. Этот фактор заставил исследователей тщательно проанализировать данные по ветровому режиму южной части Тихого океана. Однако вследствие суровых погодных условий метеонаблюдения на судах велись эпизодически. Пришлось для анализа использовать также имеющийся в НОАА массив сведений о ветрах, которые отмечались китобойными судами в прошлом веке, особенно в полосе между 40 и 50 градусами ю.ш. Эта полоса хорошо известна мореплавателям как “ревущие сороковые”, где скорость ветра превышает 70 км/ч. Обобщенные данные по ветрам были сопоставлены с концентрациями углекислого газа в поверхностных водах и приповерхностных слоях воздуха для оценки потоков поглощаемого или выделяемого углекислого газа в различных районах южной части Тихого океана. Согласно полученным результатам, в осенний сезон в Южном полушарии количество углекислого газа, выделяемого в атмосферу из океана на востоке, почти совпадает с количеством, поглощаемым океаном на западе.
Ученые допускают, что в иные сезоны южная часть Тихого океана действительно является мощным поглотителем углекислого газа. Это вопрос и практика будущего.
Следующий вопрос, который заинтересовал ученых – это механизм осаждения карбонатов в условиях фотосинтеза. Для простоты изобразим это в виде небольшого рисунка (его можно использовать как МП-картосхему на уроках химии и географии).
Рис. 2 Схема осаждения атмосферного углекислого газа, образование морских отложений.
Экспериментально изучена кинетика осаждения CaCO3 при 20°C и 30°C в условиях пересыщений, достигаемых при фотосинтезе в морской воде. Выяснена возможность спонтанного осаждения CaCO3 в условиях Багамской Банки.
Проблема осаждения карбоната кальция в океане привлекает внимание исследователей в течение последних 40 лет. Две основные точки зрения – о выделении CaCO3 исключительно биогенным путем и о спонтанном физико-химическом осаждении непосредственно из морской воды – имеют подтверждения как в экспериментальных работах, так и в результатах натуральных наблюдений. Особенно большое значение придается этой проблеме в связи с интенсивным осаждением карбонатных илов на Багамской Банке, Персидском заливе, которое часто рассматривают в качестве аналога карбонатообразования в древних морях.
Эксперименты по этому вопросу были проведены московскими учеными О.С. Покровским и В.С. Савенко (МГУ им.М.В. Ломоносова). Что же им удалось получить и изучить?
В экспериментах по изучению спонтанного физико-химического осаждения CaCO3 в морской воде была показана возможность непосредственного осаждения карбоната кальция в условиях морской воды, отвечающих районам интенсивного карбонатонакопления. Данные по Багамской Банке подтверждают действие механизма прямого физико-химического осаждения из морской воды. Но имеются многочисленные данные, которые доказывают основную роль в выделении CaCO3 сине-зеленых водорослей. В ходе фотосинтеза происходит значительное увеличение pH, что может приводить к химическому осаждению CaCO3 на внешних поверхностях клеток. Наблюдения показали, что суточные изменения pH в непосредственной близости от скоплений водорослей могут достигать 7,4 – 9,2, что приводит к выпадению CaCO3.
Несмотря на большую роль водного фотосинтеза в осаждении карбонатов, физико-химический анализ этого процесса не проводился, а имеющиеся данные по гомогенному осаждению CaCO3 не могут быть непосредственно использованы в силу изменения концентраций неорганического углерода, растворенных фосфатов, pH, происходящих при фотосинтезе.
Рассмотрим теоретически изменения состава среды, непосредственно примыкающей к фотосинтезирующим клеткам. При фотосинтезе, вследствие реакций образования электронейтральных органических соединений происходит компенсационное выделение ионов OH-, что сопровождается увеличением pH и переходом части ионов HCO3- в CO32-
n H2CO3 ® (CH2O)n + n O2;
n HCO3- + n H2O ® (CH2O)n + n O2+ n OH-;
n CO32- + 2n H2O ® (CH2O)n + n O2+ 2n OH-;
Используя условие электронейтральности – постоянство общей щелочности – Alk
Alk = [HCO3-] + 2[CO32-] + [H2BO3]- + [OH]-
и смешанные константы диссоциации, можно выразить общую концентрацию неорганического углерода Ст как функцию активности ионов водорода (10-pH)
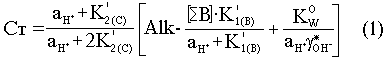
Необходимо знать, что в ходе водного фотосинтеза изменение концентрации ионов CO32- слагается из двух одновременно действующих и противоположно направленных процессов: уменьшением общего количества растворенного неорганического углерода Ст, который расходуется на синтез органических соединений, и увеличением концентрации CO32- в результате подщелачивания среды:
HCO3- + OH- ® CO32- + H2O
Это указывает на существование экстремального пересыщения, выше которого происходит снижение пересыщения при дальнейшем развитии фотосинтеза. Используя уравнение для пересыщения
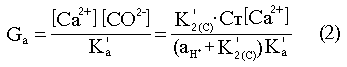
|
Alk, M |
[SB], M |
[Ca2+], M |
K'2(C) |
K11(B) |
K0w |
g*OH- |
K'arag |
|
|
20°C |
2,4·10-3 |
4,3·10-4 |
0,01 |
6,59· ·10-10 |
1,9·10-9 |
6,81· ·10-15 |
0,218 |
7,14· ·10-7 |
|
30°C |
2,4·10-3 |
4,3·10-4 |
0,01 |
8,76· ·10-10 |
2,26· ·10-9 |
1,44· ·10-14 |
0,202 |
7,65· ·10-7 |
Табл.5 Расчетные параметры для уравнений (1) и (2),
где [ ] – концентрации; K'a – концентрационное произведение растворимости арагонита, являющегося основной фазой выпадающего из морской воды карбоната кальция – можно рассчитать зависимость пересыщения от pH.
В таблице 5 приведены значения расчетных параметров в уравнениях (1) и (2) для морской воды с соленостью 35%. При температурах 20°C и 30°C, охватывающих интервал поверхностных вод с наиболее интенсивным фотосинтезом. На рис. 3,а представлена кривая снижения концентрации растворенного углерода в системе в ходе фотосинтеза, а на рис. 3,б – зависимость пересыщения от интенсивности фотосинтеза (величины pH).
Как видно из этих рисунков, полного выделения растворенной углекислоты в фотосинтезирующих природных системах не происходит. Максимальное значение пересыщения – 11 – 12 раз по арагониту достигается уже при величинах pH = 9,2 – 9,4, реализуемых в природной обстановке.
Поскольку уравнения зависимости индукционного периода осаждения CaCO3 от пересыщения относятся к условиям морской воды с Ст = 2,33 ммоль/л = const, нельзя считать, что выведенные закономерности напрямую приложимы к условиям фотосинтеза. Дополнительным фактором неопределенности является влияние фосфат-ионов – главных ингибиторов осаждения CaCO3 в природе. Закономерное выведение фосфора из раствора через пищевые цепи организмов может сильно изменить оценку скорости осаждения карбоната кальция.
Были проведены и специальные исследования по изучению кинетики спонтанного осаждения карбоната кальция в условиях, моделирующих фотосинтез в морской воде. В отличие от более ранних экспериментов, в этой работе проводились по два параллельных опыта при индукционных периодах менее 500 минут, что позволило снизить относительную ошибку измерений до 10%. Величины индукционных периодов осаждения определяли визуально или спектрофотометрически. В слабопересыщенных растворах, в силу трудности обнаружения малого количества осадка, основным критерием с начала осаждения было уменьшение pH на заранее заданную величину. Дополнительный контроль карбонатной щелочности, измеренной в нескольких пробах, отфильтрованных через мембранный фильтр после окончания индукционного периода, показал ее заметное уменьшение. Это подтверждает надежность критерия снижения pH в качестве мер индукционного периода. Эксперименты проводили в закрытой ячейке при 20±0,5°C и 30±0,1°C, термостатируемой с помощью водного термостата U15. Во всех опытах использовали искусственную морскую воду соленостью 35%, отфильтрованную сначала через бумажный фильтр, а затем через мебрану 0,45 мм.
Варьирование концентрации общего углерода достигали путем смешивания двух растворов морской воды: без HCO3- и содержащей 10 ммоль/л NaHCO3. Далее в раствор с известной концентрацией общего углерода добавляли несколько капель раствора NaOH до создания величины pH, отвечающей данному Ст в соответствии с уравнением (1) и рис.3. Фосфат вводили в виде точной аликвоты свежеприготовленной морской воды, содержащей 10-5 M PO43-.
Смотрите также
Статистическая термодинамика
Термодинамическая система, коллектив и его
состояния. Метод ансамблей. Энтропия и вероятность. Канонический ансамбль
Гиббса. Каноническое распределение. Фактор Гиббса. Вероятности, свободная ...
Поливинилпирролидон:
его применение и важнейшие характеристики
Поливинилпирролидон является виниловым полимером. В основном его получают
методом радикальной виниловой полимеризации из мономера винилпирролидона. ...
