НитрованиеМатериалы / Методы органического синтеза / НитрованиеСтраница 1
Введение нитрогруппы – NO2 в молекулы органических соединений. Может проходить по электрофильному, нуклеофильному и радикальному механизмам; активные частицы в этих реакциях – соответственно катион нитрония NO2, нитрит-ион NO2 и радикал NO2. Нитрование может осуществляться по атомам С, N, О замещением атома водорода (прямое нитрование) или других функциональных групп (заместительное нитрование) либо в результате присоединения группы NO2 по кратной связи.
Электрофильное нитрование.
Среди электрофильных нитрующих агентов доминирующее положение занимает HNO3. Безводная и конц. HNO3 способны к самопротонированию: 2HNO3![]() [Н2NО3]+ + NO3-
[Н2NО3]+ + NO3- ![]() NО2+ + NO-3 + H2O. Присутствие воды снижает концентрацию NO+2 и в 93 – 95%-ной HNO3 спектрофотометрически он уже не обнаруживается. Для увеличения нитрующей активности HNO3 используют ее смеси с H2SO4 или олеумом, к-рые генерируют NO2, связывая воду:
NО2+ + NO-3 + H2O. Присутствие воды снижает концентрацию NO+2 и в 93 – 95%-ной HNO3 спектрофотометрически он уже не обнаруживается. Для увеличения нитрующей активности HNO3 используют ее смеси с H2SO4 или олеумом, к-рые генерируют NO2, связывая воду:
![]()
В безводной H2SO4 при содержании HNO3 меньше 10% равновесие полностью сдвинуто вправо. Применяют также комбинации HNO3, разложение оксидов азота и органических нитратов с кислотами Льюиса (АlСl3, ZnCl2, BF3 и др.); сильным нитрующим действием обладает смесь HNO3 с (СН3СО)2О благодаря образованию ацетилнитрата и N2O5 (последний при содержании в смеси более 90% HNO3 полностью диссоциирует на NO+2 и NO-3); перспективны также смеси HNO3 с безводным SO3 или N2O5. Вместо HNO3 можно применять ее соли, однако в промышленности такой метод не используют из-за осложнения процесса регенерации отработанных к-т. В случае слабой взаимной р-римости нитрующего агента и субстрата, а также для уменьшения побочных процессов нитрование проводят в органических р-рителях, например нитрометане, сульфолане, уксусной к-те; полярные р-рители способствуют диссоциации [H2NO3]+ и тем самым увеличивают концентрацию NO2.
В лабораторной практике широко используют апротонные нитрующие агенты (нитраты, соли нитрония, полинитросоед. и др.), активность которых в реакциях электрофильного нитрования увеличивается в ряду: AlkONO2 < (CH3)2C(CN) ONO2 < < RC(N02)3 ![]() RN(N02)2 < NO2F < CH3COONO2 < < N2O5 < NO2+X-.
RN(N02)2 < NO2F < CH3COONO2 < < N2O5 < NO2+X-.
Субстратами для электрофильного нитрования служат ароматические и гетероциклические соединения, олефины, относительно сильные СН – кислоты, амины, спирты.
Нитрование ароматического соединения протекает по схеме:
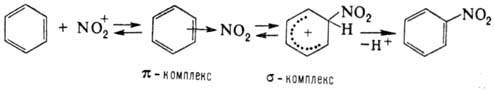
Возможно также образование s‑комплекса, в котором группа NO2 связана с атомом углерода кольца, несущим заместитель. Соединения с электронодопорными заместителями более реакционноспособны и нитруются в орто- и пара-положения, а с электроноакцепторными – в мета-положение. В промышленности для нитрования ароматических соединений применяют в основном смесь HNO3 и H2SO4 (выход нитропродуктов ~ 90–95%). Основная побочная р-ция – окисление, приводящее, как правило, к деструкции ароматического кольца. В зависимости от реакционной способности субстрата условия нитрования варьируют в широких пределах – от водной HNO3 при 0 °С (обязательно присутствие оксидов азота) до дымящей HNO3 в олеуме при повышенных температурах. При низких температурах с высокой скоростью протекает нитрование ароматических соединений солями нитрония; при этом часто лимитирующая стадия-скорость растворения соли нитрония. Используют также заместительное нитрование – замещение сульфо-, диазо- и др. функциональных групп. Этим приемом пользуются, в частности, в случаях, когда невозможно прямое нитрование. Нитрование олефинов апротонными нитрующими агентами в зависимости от условий и строения реагентов может идти по разным направлениям, включая отщепление Н+, присоединение элементов р-рителя и противоиона, полимеризацию и др., например:
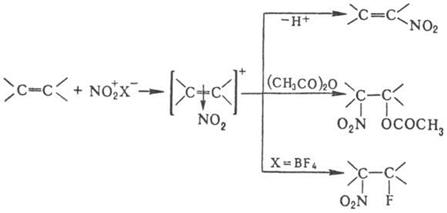
При нитровании олефинов тетранитрометаном в зависимости от строения олефина образуются либо алифатическое полинитро – соединение, либо производные изоксазолидина, например:
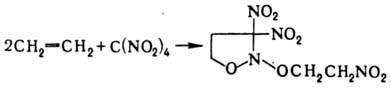
Некоторые СН – кислоты при нитровании образуют анионы соответствующих нитросоединений; например, при действии на флуорен этил – нитрата в присутствии С, Н5ОК образуется К – соль 9‑нитро-флуорена, примером нитрования карбанионов может служить также превращение солей моно- и динитросоединений соответственно в геминальные ди- и тринитропроизводные при действии FNO2. Соединения с активированной метиленовой группой можно нитровать и в кислых условиях; например, при обработке диэтилмалоната HNO3 образуется нитродиэтилмалонат, нитрование в аналогичных условиях 1,3 – индандиона с последующим щелочным гидролизом образующегося a – нитрокетона – удобный метод синтеза первичных нитроалканов:
Смотрите также
Теория хроматографии, хроматографический анализ, виды хроматографии
...
Введение
Свою дипломную работу хочу
начать со слов ученого-земляка М.В. Ломоносова, которые являются эпиграфом
данной работы:
“Вольность и союз наук необходимо
требуют взаимного сообщения и беззавистного ...
Совершенствование технологии получения технического ПАН жгутика
Полиакрилонитрильные
волокна и нити в настоящее время представляют наиболее распространенный вид
промышленно освоенных карбоцепных синтетических волокон. Это связано со
специфически ценными ...
