Циклическая вольтамперометрияМатериалы / Электроаналитические методы в аналитической химии / Циклическая вольтамперометрия
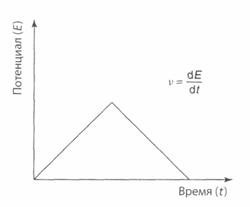
По мере восстановления на поверхности электрода окисленной формы Ох образуется восстановленная форма R, которая переходит обратно в раствор. При обратной развертке потенциала вблизи значения Е, равного окислительно-восстановительному потенциалу пары Ox-R, восстановленная форма вновь окисляется с образованием Ох. Ток при этом начинает возрастать в противоположном направлении до тех пор, пока не достигнет пикового значения. Подобный метод исследования называют циклической вольтамперометрией. На рисунке показано, как в этом методе изменяется наложенный на электроды потенциал в зависимости от времени.
Как сделать ежедневник своими руками кожаный ежедневник своими руками www.yaom.ru.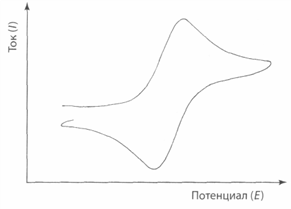
На типичной циклической вольтамперограмме видны два пика. Один из них отражает восстановление исходной окисленной формы, а другой - реокисление восстановленной формы с образованием исходного вещества. Пиковые токи практически одинаковы по величине, а соответствующие им потенциалы сдвинуты друг относительно друга на 0,056/nВ. Независимо от концентрации Ох, коэффициентов диффузии или скоростей электронного переноса, среднее арифметическое этих потенциалов равно стандартному окислительно-восстановительному потенциалу Е° пары Ox-R.
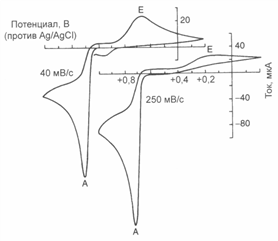
В том случае, если превращение на электроде протекает необратимо, пики будут сдвинуты друг относительно друга на большую величину: Eр(с) - Ep(a) > 0,056/n В. Однако и в этом случае среднее арифметическое пиковых потенциалов с хорошим приближением можно считать за Е°. Бывают случаи, когда обратный пик не возникает вовсе, либо он сильно отличается по форме от прямого пика. Обычно это указывает на полную необратимость процесса восстановления Ох за счет дальнейших превращений восстановленной формы R. В качестве примера можно привести циклическую вольтамперограмму 4-ацетиламинофенола (парацетамола) - вещества, легко окисляющегося наугольно-пастовом электроде.
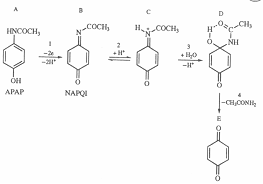
Пик, соответствующий окислению парацетамола, направлен вниз. При обратной развертке потенциала второй пик, отражающий электрохимическое восстановление, возникает на значительном удалении и гораздо шире первого. Подобные вольтамперограммы получены при трех скоростях развертки и при трех разных значениях рН. Их подробный а нализ позволил установить природу протекающих в электрохимической ячейке превращений.
Смотрите также
Введение
Свою дипломную работу хочу
начать со слов ученого-земляка М.В. Ломоносова, которые являются эпиграфом
данной работы:
“Вольность и союз наук необходимо
требуют взаимного сообщения и беззавистного ...
Применение информационных технологий в процессе обучения химии
Известно, что образование - один из главных институтов
социализации личности. Главная цель образования - формирование свободной,
ответственной, гуманной личности, способной к дальнейшему сам ...
Ртуть (Hydrargyrum), Hg
Каждому, кто хоть раз держал в руках термометр - "градусник", знакома ртуть. По своим химическим свойствам - это настоящий металл, но в отличие от других металлов жидкий при комнатной темпер ...
