Способы определения порядка реакции и константы скорости. Способ
избыточных концентрацийМатериалы / Скорость образования, расходования компонента и скорость реакции / Способы определения порядка реакции и константы скорости. Способ
избыточных концентраций
Для реакции
v1А1 + v2A2→Продукты (22)
зависимость скорости от концентрации исходных веществ записывается уравнением:
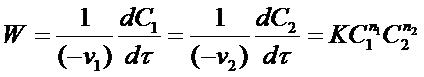 (23)
(23)
где С1 и С2 - концентрации исходных веществ А1 и А2;
п1 и п2 - порядки реакции по веществам А1 и А2;
К - константа скорости реакции. Общий (суммарный) порядок реакции равен:
п = п1 + п2 (24)
Если реакция элементарная и формально простая и подчиняется кинетическому уравнению для элементарных реакций, то порядок реакции по веществам А1 и А2 равен их стехиометрическим коэффициентам в уравнении реакции, то есть
п1=v1 и п2=v2
тогда п = v1+ v2
Для определения порядка химической реакции сначала, по экспериментальным результатам изменения концентрации исходных веществ со временем, находят порядки реакции по веществам. Затем общий порядок реакции.
Для того чтобы скорость реакции зависела в явном виде только от концентрации одного из исходных веществ, обычно используют способ избыточных концентраций или метод изолирования Оствальда
.
Он заключается в следующем.
Сначала проводят реакцию, когда концентрация исходного вещества А2 избыточна по сравнению с веществом А1. При протекании реакции считают, что меняется только концентрация вещества А1 (обычно она в 10 .1000 раз меньше концентрации остальных веществ), а концентрация вещества А2 практически постоянна и её можно ввести в постоянный коэффициент. При этом уравнение (23) примет вид:
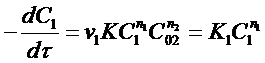 (25)
(25)
где 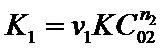 - константа скорости реакции по веществу А1.
- константа скорости реакции по веществу А1.
Затем проводят реакцию при избытке вещества А1 по сравнению с веществом А2. Тогда уравнение (23) преобразуется к виду:
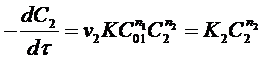 (26)
(26)
где ![]() - константа скорости реакции по веществу А2.
- константа скорости реакции по веществу А2.
Если удастся определить величины п1 и п2 , то можно будет найти общий порядок реакции по формуле (24) и константы скорости К1 и К2 , а затем константу скорости реакции по формуле:
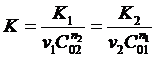
Иногда при проведении опытов используют метод, в котором концентрацию одного из исходных веществ изменяют, а концентрацию другого вещества оставляют постоянной.
Способы расчета порядка реакции по данному веществу подразделяются на дифференциальные и интегральные. Рассмотрим некоторые из них.
Смотрите также
Химический язык
В условиях развития современного общества
повышаются требования к качеству обучения школьников, уровню знаний и умений
учащихся. При том, резко возрастает нагрузка на весь образовательный пр ...
Теплопроводность в сплошных средах и двухфазных, продуваемых и непродуваемых телах (слоях)
...
Приложение 1
Конкретные
примеры о методах реализации межпредметных связей.
1. Вопросы
межпредметного содержания:
а) Вспомните (из
курса географии) основные месторождения в России:
· алмаза
· поваре ...
