Обратимые реакцииМатериалы / Кинетика химических реакций / Обратимые реакции
В химических реакциях исходные вещества не всегда полностью превращаются в продукты реакции. Это происходит потому, что по мере накопления продуктов реакции могут создаваться условия для протекания обратимой реакции в противоположном направлении.
Например, если смешать пары иода с водородом при температуре 200°
С, то произойдет реакция:
![]()
Однако известно, что йодистый водород уже при нагревании до 180 °С начинает разлагаться на иод и водород:
![]()
Понятно, что в этих условиях не произойдет ни полного разложения НI, так как продукты реакции способны вновь реагировать между собой, ни полного образования йодистого водорода. Химические реакции, которые при одних и тех же условиях могут идти в противоположных направлениях. называются обратимыми.
При написании уравнений обратимых реакций вместо знака равенства ставят две противоположно направленные стрелки. Уравнение рассмотренной выше обратимой реакции запишется следующим образом:
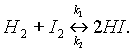
Реакцию, протекающую слева направо называют прямой (константа скорости прямой реакции k1), справа налево — обратной (константа скорости обратной реакции k2).
Смотрите также
Технеций (Technetium), Те
Технеций был предсказан как эка-марганец Менделеевым на основе его Периодического закона. Несколько раз он был ошибочно открыт (как люций, ниппоний и мазурий), настоящий технеций был открыт в 1937 год ...
Соединения азота
Анализ содержания экспериментальной части программы
по данной теме свидетельствует, что большинство продуктов реакций являются
минеральными удобрениями. Утилизировать отходы можно по следующ ...
