Сущность
и природа водородной связиМатериалы / ИК-спектральное проявление водородных связей / Сущность
и природа водородной связиСтраница 1
Первую научную трактовку водородной связи дали в 1920 году В. Латимер и В. Родебуш, работавшие в лаборатории Г. Льюиса, основоположника учения о ковалентной связи, автора теории кислот и оснований и плодотворной в органической химии концепции обобщенной электронной пары. Причину особых физических и химических свойств воды авторы объясняли наличием водородной связи, сущность которой состоит во взаимодействии атома водорода одной молекулы с электронной парой атома кислорода другой молекулы. При этом атом водорода становится одновременно связанным с двумя атомами кислорода ковалентной и водородной связью(2).
За все последующее время вплоть до наших дней не изменился принципиальный подход к трактовке водородной связи, концепция неподеленного протона осталась незыблемой. Длительные и интенсивные исследования позволили уточнить влияние структуры соединений на склонность к образованию Н-связей, внесена определенная ясность в электронную природу последних, найдены надежные методы их идентификации. А главное – сделаны широкие обобщения по оценке влияния Н-связей на физические и химические свойства веществ. Бутлеровский тезис “структура определяет свойства” раскрывается с учетом возможности образования Н-связи и ее вклада в конкретные свойства.
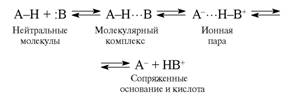
По современной терминологии, образование водородной связи наступает при взаимодействии протонодонора (кислоты Бренстеда, электроноакцептора) с протоноакцептором (основанием, электронодонором). Водородную связь можно представить как невалентное взаимодействие между группой А – Н одной молекулы и атомом В другой, в результате которого образуется устойчивый комплекс А – Н….В с межмолекулярной водородной связью, в котором атом водорода играет роль мостика, соединяющего фрагменты А и В. Но нужно заметить , что до настоящего времени нет однозначного подхода , какую конкретно связь называть водородной. Большинство авторов к понятию водородной связи относят дополнительное взаимодействие, которое возникает между атомом водорода и электронодонором В, то есть связь Н….В. Другие авторы к понятию водородной связи относят всю цепочку Х – Н….В, то есть связь между атомами Х и В через водородный мостик. Образование водородной связи может быть представлено как кислотно – основное взаимодействие, определяющее первую стадию переноса протона при протолитических реакциях
 |
Экспериментальные факты, сопровождающие процесс образования водородной связи:
1. При образовании водородных связей выделяется теплота – термохимическая мера энергии Н-связи. Эту характеристику используют для калибровки спектральных методов изучения водородных связей.
2. Расстояние между соседними атомами, участвующими в образовании водородной связи, значительно меньше суммы их ванн-дер-ваальсрвых радиусов. Последнее обстоятельство является одним из критериев, указывающих на образование между молекулами водородных связей.
3. Водородная связь увеличивает длину связи Х-Н, что приводит к смещению соответствующей полосы валентных колебаний в ИК-спектре в сторону более низких частот. Метод ИК-спектроскопии является главным методом изучения водородной связи.
Современная ИК-спектроскопия представляет собой экспресс-метод установления структурных особенностей органических соединений. С помощью ИК-спектроскопии быстро и надёжно идентифицируются разнообразные функциональные группы: карбонильная, гидроксильная, карбоксильная, амидная, амино, циано и др.; а также различные непредельные фрагменты: двойные и тройные углерод-углеродные связи, ароматические или гетероароматические системы. Методами ИК-спектроскопии изучают внутри- и межмолекулярные взаимодействия, например, образование водородных связей. В химии древесины и химии природных соединений с помощью ИК-спектроскопии исследуют структуры углеводов, лигнинов, аминокислот, терпенов, стероидов и многих других веществ.
Смотрите также
Химики создали молекулу, способную удалять из раствора отрицательно заряженные ионы
Химики создали органическую молекулу, способную связывать отрицательно заряженные ионы растворенных веществ. Это позволяет очищать растворы от ионов, например, хлора и фтора.
Агенты (вещества), спос ...
Классификация, количественные определения минеральных удобрений
Минеральные удобрения
— это соединения, способные при внесении в почву растворяться и диссоциировать
на ионы в почвенном растворе, чрезвычайно необходимые для жизни растений,
поскольку соде ...
Заключение.
Целью моего реферата было
изучение общих сведений о комплексных соединениях,
более детально рассмотреть строение.
Комплексные соединения составляют наиболее обширный и
разнообразный класс неорга ...
