Физико-химические основы синтеза азотной кислоты из аммиакаСтатьи / Производство азотной кислоты / Физико-химические основы синтеза азотной кислоты из аммиакаСтраница 2
![]() (7)
(7)
и зависит от таких параметров процесса как температура (через Км), давление и состав АмВС, то есть отношение кислород: аммиак (через АС), время контактирования, то есть время пребывания АмВС в зоне катализатора. Влияние этих факторов на скорость окисления аммиака до оксида азота (II) по реакции 1 и до азота по реакции 3 и, следовательно, выход продуктов окисления, различно.
4.1. Температура. Повышение температуры способствует увеличению скорости реакций и коэффициента диффузии аммиака в смеси и, поэтому, является наиболее эффективным средством, увеличения скорости процесса, протекающего преимущественно в диффузионной области. Это подтверждается термодинамическими данными табл. 15.1.
Термодинамические характеристики реакций окисления аммиака
Таблица 4.1.
|
Реакция |
ΔН, Дж/моль |
AG, кДж/моль | |
|
298°К |
1173оК | ||
|
4NH3 + 502 = 4NO + 6Н20 |
-226,0 |
-246,2 |
-414,6 |
|
4NH3 + 302 = 2Н2 + 6Н20 |
-317,2 |
-326,9 |
-335,2 |
Из таблицы следует, что вероятность реакции окисления до оксида азота (II) с повышением температуры возрастает почти вдвое, а реакции окисления до азота почти не изменяется. Зависимость выхода оксида азота (II) и элементарного азота от температуры представлена на рис. 4.1.
4.2. Состав АмВС, Соотношение аммиака и кислорода в газовой смеси влияет на температурный режим и общую скорость процесса в том случае, если лимитирующей в нем является химическая реакция, то есть процесс протекает в кинетической области. При стехиометрическом соотношении компонентов в АмВС степень превращения аммиака в оксид азота (II) не превышает 0,65 дол. ед. Для увеличения выхода оксида азота (II) процесс ведут при отношении О2 : NH3 = 1,8—2,0, что соответствует содержанию в АмВС 0,095—0,105 об. долей аммиака и 0,18—0,19 об. долей кислорода. Избыток кислорода используется на стадии доокисления оксида азота (II), а указанный состав АмВС обеспечивает автотермичность процесса окисления и лежит за пределом взрывчатости АмВС. Зависимость выхода оксида азота (II) от состава АмВС представлена на рис. 4.2.
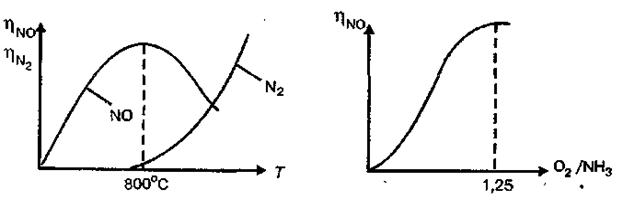
Рис. 4.1. Зависимость выхода NO и N2 Рис. 4.2. Зависимость выхода NO от температуры от состава АмВС
3. Давление. Повышение давления ускоряет процесс окисления аммиака за счет увеличения концентрации реагентов и производительности катализатора, что позволяет сократить размеры аппаратуры. При этом, однако, снижается выход оксида азота (II) и увеличивается эрозия и унос катализатора, что удорожает продукцию. Так, если при атмосферном давлении (105 Па) унос катализатора не превышает 0,05 г на тонну азотной кислоты, то при давлении 0,8 МПа он достигает 0,4 г/тонну. Зависимость выхода оксида азота (II) от давления при различной температуре приведена на рис. 4.3.
4. Время контактирования, Скорость каталитического окисления аммиака до оксида азота (II) весьма высока. За десятитысячные доли секунды степень превращения составляет 0,9 7— 0,98 дол. ед. при атмосферном давлении и 0,98—0,96 при давлении 0,8—1,0 МПа. Время контактирования может быть рассчитано из формулы:
![]() (8)
(8)
где: Vk — объем катализатора, определяемый в случае платинового катализатора числом сеток в пакете, W — объемная скорость АмВС. Время контактирования зависит от природы катализатора и составляет; для платиновых катализаторов 10-4 - 10-5с, для окисных катализаторов около
Смотрите также
Моделирование процессов разряда-ионизации серебра на поверхности твердого электрода
...
Калифорний (Californium), Cf
Получен искусственно в 1950 группой Сиборга в Калифорнийском университете в Беркли.
Назван в честь Калифорнийского университета в Беркли, где и был получен. Как писали авторы, этим названием они хотел ...
