Распределение комплексов металловПериодическая система / Методы экстракции в исследовании равновесий / Распределение комплексов металловСтраница 1
Экстрагируемость ионов металлов и комплексов металлов различными растворителями определяется многими условиями. Если лиганд заряжен и в процессе последовательного комплексообразования образуется электронейтральный комплекс, то этот комплекс может извлекаться органическим растворителем с низкой диэлектрической постоянной. Иногда этот незаряженный комплекс является последним в серии последовательно образующихся комплексов, но отмечены случаи, когда имеет место даль-
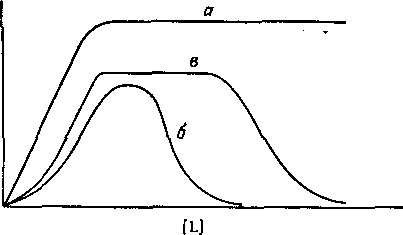
Рис. 1. Зависимость коэффициента распределения q экстрагируемого соединения от концентрации свободного лиганда.
а — образуется координационно насыщенный электроне игральны и комплекс;
6 -- а системе образуется анионный комплекс; в — образуется очень устойчивый электроне игральный комплекс с последующим образованием анионного комплекса.
нейшее присоединение лигандов с последующим образованием комплексных анионов.
В большинстве случаев анионные комплексы не экстрагируются, так что вид кривой распределения комплекса от концентрации лиганда будет разным в зависимости от того, образуется ли в системе анионный комплекс или нет. Коэффициент распределения представляет собой отношение общей концентрации металлсодержащих частиц в обеих фазах:
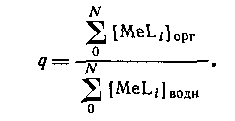
Если MeLm является единственным комплексом, присутствующим в значительных количествах в органической фазе, то
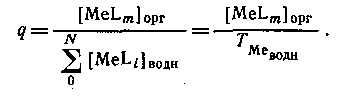
Следовательно, если m = N, то q([L]) представляет собой монотонную функцию, в то время как при N>m эта функция имеет максимум. Если устойчивость нейтрального комплекса достаточно велика, то функция q от [L] имеет отчетливо выраженное плато. Учитывая, что константа распределения соединения MeLm определяется уравнением
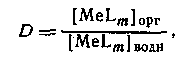
концентрацию MeLm в водной фазе можно определить, вводя константу устойчивости:
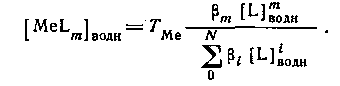
Следовательно,
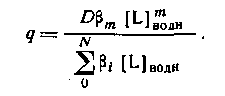
Из уравнения следует, что для расчета N неизвестных констант устойчивости необходимо по крайней мере N+1 экспериментов по распределению. Если кривая распределения имеет длинный горизонтальный отрезок, то значение D непосредственно определяется значением qmax.
D = qmax
Константы устойчивости наиболее просто определяются в том случае, когда функция q от [L] имеет максимум, так как в этом случае образование катионных и анионных комплексов можно рассматривать отдельно.
Этот принцип впервые был использован Морзе при изучении галогенидных комплексов ртути(П); фундаментальные проблемы определения и расчета констант устойчивости были рассмотрены Ридбергом, Дирсеном и Ирвингом.
Если при изучении данной системы комплексов используются различные органические растворители, то, как следует из уравнения, должны быть получены одни и те же константы устойчивости. Если разность между константами устойчивости превышает ошибку эксперимента, то это свидетельствует о взаимодействии между экстрагируемым комплексом и молекулами растворителя. Такое взаимодействие приводит к изменению значения q. В соответствии с рис. 2 отношение qCHCl3/qC6H6 при экстракции ацетилацетоната тория (IV) остается постоянным при одинаковых концентрациях свободного лиганда, но отношение qC6H6 /qC4H9COCH3 существенно меняется. Такое поведение было количественно объяснено образованием смешанного комплекса тория с ацетилацетоном и метилизобутилкетоном.
Смотрите также
Селен (Selenium), Se
Селен - химический элемент VI группы периодической системы Менделеева; атомный номер 34, атомная масса 78, 96; преимущественно неметалл. Природный С. представляет собой смесь шести устойчивых изотопов ...
Сера (Sulfur) S
Сера известна человеку со времен глубокой древности. Легендарный древнегреческий поэт Гомер, живший между XII и VIII вв. до нашей эры, автор эпических поэм "Иллиада" и "Одиссея&qu ...
Углеводы
Углеводы на ряду с белками и липидами
являются важнейшими химическими соединениями живых организмов. В организме
углеводы выполняют важнейшие функции: энергетическую, структурную, защитн ...
