Химические свойства углекислого газаПериодическая система / Межпредметные связи в курсе школьного предмета химии на предмете углерода и его соединений / Химия элемента углерода и его
соединений / Химические свойства углекислого газа
Оксид углерода (IV) химически довольно активен. Рассмотрим некоторые реакции.
1. Оксид углерода (IV) – кислотный оксид, ему соответствует двухосновная угольная кислота. Растворение оксида углерода (IV) – обратимая реакция.
H2O + CO2 ![]() H2CO3
H2CO3
равновесие при комнатной температуре на 99% сдвинуто влево
Углекислый газ не просто растворяется в воде, а частично соединяется с нею, образуя угольную кислоту.
2H2O + CO2 ![]() H3O+ + HCO3-
H3O+ + HCO3-
Однако угольная кислота – соединение крайне непрочное. Она может присутствовать лишь в водном растворе, при всякой же попытке выделить угольную кислоту из раствора она опять разлагается на CO2 и H2O.
H2CO3 ![]() H+ + HCO3 KaI = 4,45·10-7
H+ + HCO3 KaI = 4,45·10-7
HCO3- ![]() H+ + CO3 KaII = 4,69·10-11
H+ + CO3 KaII = 4,69·10-11
2. С сильными основаниями оксида углерода (IV) реагирует с образованием солей угольной кислоты – карбонатов и гидрокарбонатов.
Ca(OH)2 + CO2 ® CaCO3¯ + H2O
CaCO3 + H2O + CO2 ® Ca(HC03)2
3. Углекислый газ – вещество очень прочное, тем не менее при температуре красного каления с кальцием дает карбид и оксид кальция.
2CO2 + 5Ca ® CaC2 + 4CaO
4. Наиболее активные металлы горят в оксиде углерода (IV).
600°C
2Mg + CO2 ® 2MgO + C
5. При высоких температурах восстанавливается в CO с железом, цинком, углем.
3CO2 + 4Fe ® 2Fe2O3 + 3C
CO2 + C ® 2CO
6. С водородом в присутствии никеля при 350-400°C или оксида меди (II) при 200°C восстанавливается в метан.
350-400°C
CO2 + 4H2 ® CH4 + 2H2O
Ni
7. С аммиаком при 600°C дает карбамид.
CO2 + NH3 ® CO(NH2)2
8. С сероуглеродом в присутствии меди дает
CO2 + CS2 ® 2S + 2CO
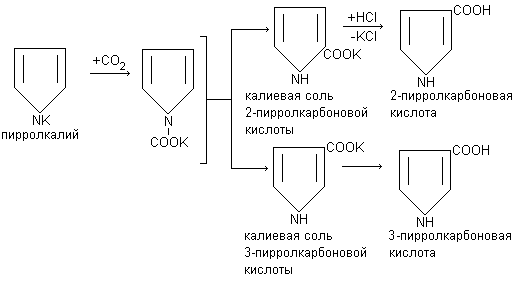
9. Реагирует со многими органическими соединениями, карбоксилируя их. Пиррол, подобно фенолу карбоксилируется оксидом углерода (IV), образуя 2-пирролкарбоновую кислоту, а в более жестких условиях температуры 3-пирролкарбоновую кислоту.
Смотрите также
Свидетельство Никола Фламеля
(Существует несколько версий истории Никола Фламеля, рассказанной им самим. Они
изложены у Уэйта в «Алхимиках сквозь века», у Кокрена в «Алхимии — заново открытой
и восстановленной в правах» и у С ...
Никель (Niccolum), Ni
Никель - химический элемент первой триады VIII группы периодической системы Менделеева, атомный номер 28, атомная масса 58,70; серебристо-белый металл, ковкий и пластичный. Природный Н. состоит из сме ...
Тепловой эффект химической реакции
Тепловые
эффекты химических реакций необходимы для многих технических расчетов. Они
находят обширное применение во многих отраслях промышленности, а также в
военных разработках.
Целью
д ...
