Уравнение ФрейндлихаПериодическая система / Лекции по коллоидной химии / Уравнение Фрейндлиха
Теоретические представления, развитые Ленгмюром и Поляни, в значительной степени идеализируют и упрощают истинную картину адсорбции. На самом деле поверхность адсорбента неоднородна, между адсорбированными частицами имеет место взаимодействие, активные центры не являются полностью независимыми друг от друга и т.д. Все это усложняет вид уравнения изотермы. Г. Фрейндлих предположил, что число молей адсорбированного газа или растворенного вещества, приходящееся на единицу массы адсорбента (т.н. удельная адсорбция x/m) должна быть пропорциональна равновесному давлению (для газа) или равновесной концентрации (для веществ, адсорбируемых из раствора) адсорбента, возведенной в некоторую степень, которая всегда меньше единицы:
![]() (IV.15)
(IV.15)
![]() (IV.16)
(IV.16)
|
) |
) |
Рис. 4.7Изотерма адсорбции Фрейндлиха в обычных (а) и логарифмических (б) координатах
Показатель степени n и коэффициент пропорциональности а в уравнении Фрейндлиха определяются экспериментально. Логарифмируя уравнения (IV.15 - IV.16), получаем:
![]() (IV.17)
(IV.17)
![]() (IV.18)
(IV.18)
Т.о., зависимость логарифма удельной адсорбции от логарифма концентрации (давления) графически выражается прямой линией, отсекающей на оси ординат отрезок, равный lg
a, тангенс угла наклона которой к оси абсцисс равен по величине показателю степени при давлении или концентрации (рис. 4.7):
![]() (IV.19)
(IV.19)
Смотрите также
Сравнительный анализ: методы получения синтез-газа
...
Ионообменная хроматография
В ионообменной хроматографии
разделение компонентов смеси достигается за счет обратимого взаимодействия
ионизирующихся веществ с ионными группами сорбента. Сохранение
электронейтральности с ...

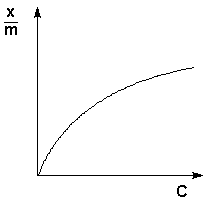 (а
(а
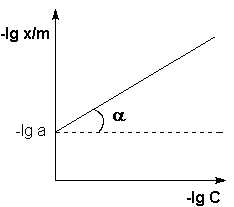 (б
(б