МалахитМатериалы / МалахитСтраница 6
Следовательно, запись (CuOH)2CO3 – основная соль, дигидроксикарбонат меди(II) – наиболее полно отражает состав малахита.
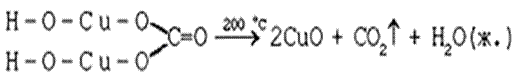
Рассмотрим реакцию разложения малахита:
https://kovka116.ru отзывы о ковка казань.(CuOH)2CO3 →2CuO +H2O + CO2
В зависимости от этапа изучения химии она может быть описана:
а)
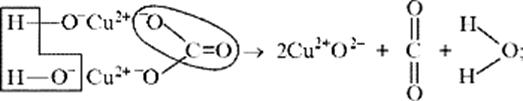
б) на ионно-структурном уровне:
в) на электронно-ионном уровне:
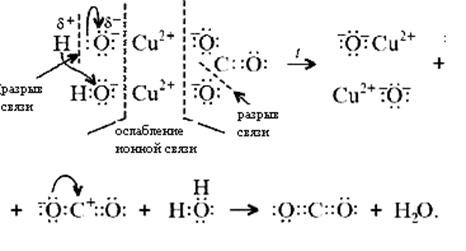
Знание свойств карбонатов и нерастворимых в воде оснований позволяет утверждать, что малахит будет растворяться в кислотах:
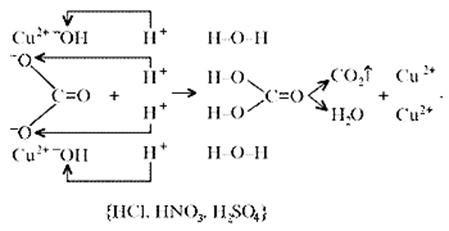
Примечание. Ион Н+ присоединяется к кислороду в составе гидроксид- и карбонат-ионов по донорно-акцепторному механизму:
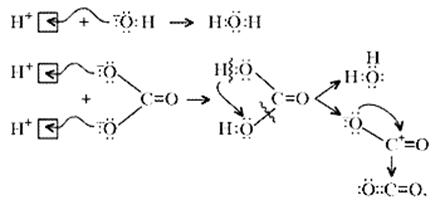
Малахит можно рассматривать как производное гидроксида меди(II), в котором часть гидроксильных ионов замещена на карбонат-ионы (таково, собственно, определение понятия «основная соль»). Кроме реакции с кислотами при определенных условиях он может реагировать с кислотными оксидами. Мысль совершенно невероятная, учитывая нерастворимость малахита в воде – главнейшее условие взаимодействия кислотных оксидов с основаниями, точнее со щелочами. Однако имеет место реакция:
(CuOH)2CO3 + CO2 = CuCO3)2 + Н2О
«Химические события» соответствуют такому механизму:
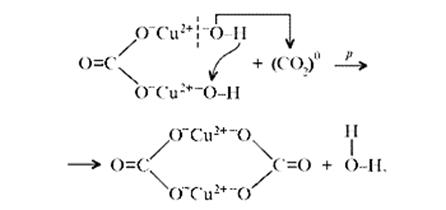
Обратим внимание на образование средней соли. Теперь считается доказанным, что карбонат меди(II) можно помещать в список солей угольной кислоты.[11] Малахит, как известно, не растворяется в воде, но может подвергаться гидролизу (из-за гидролиза, собственно, невозможно получить осадок среднего карбоната меди):
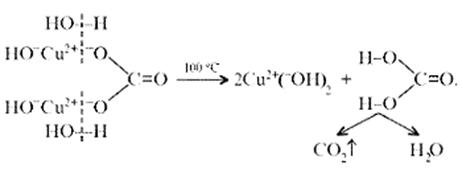
Из-за способности ионов меди образовывать комплексные ионы малахит растворяется, в частности, в карбонатах щелочных металлов:
(CuOH)2CO3 + K2CO3 = K2[Cu(CO3)2] + Cu(OH)2.
темно-синий
Теоретическим обоснованием этому может служить запись:
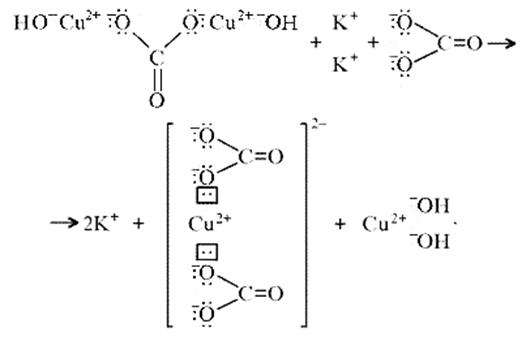
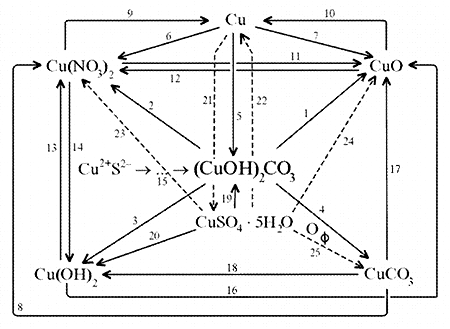
Схема генетических связей: образование и свойства малахита.
|
|
1. Разложение малахита. 2. Растворение малахита в кислотах. 3. Гидролиз малахита. 4. Реакция с углекислым газом. 5. Коррозия меди на воздухе (образование зеленого налета на медных предметах во влажном воздухе):
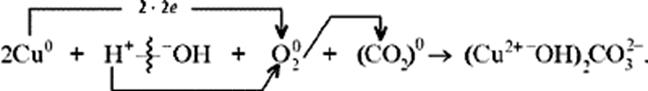
6. Растворение меди в азотной кислоте. 7. Прокаливание меди на воздухе. 8. Взаимодействие твердого тела карбоната меди(II) c крепким раствором азотной кислоты. 9. Восстановление меди из ее соли более активным металлом или в результате электролиза. 10. Восстановление меди из ее оксида водородом или другим удобным восстановителем (монооксид углерода, древесный уголь). 11. Нагревание твердого тела нитрата меди(II) до полного разложения. 12. Растворение оксида CuO в концентрированной азотной кислоте. 13. Нейтрализация основания Cu(OH)2 азотной кислотой. 14. Взаимодействие нитрата меди(II) с раствором щелочи. 15. Образование малахита в природных условиях. В самых общих чертах генезис сложных геохимических процессов можно представить так:
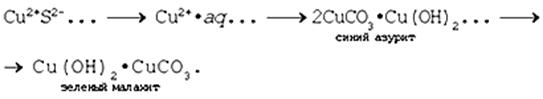
16. Нагревание твердого вещества Cu(ОН)2 (несильно, чтобы не перевести оксид CuO в оксид Cu2O) до полного разложения. 17. Нагревание CuCO3 до полного разложения на CuO и СО2. 18. Гидролиз карбоната меди(II). 19. Получение порошкообразного малахита в лабораторных условиях. Формально химизм образования дисперсного малахита можно выразить следующими уравнениями:
Смотрите также
Америций (Americium), Am
Америций - искусственно полученный радиоактивный химический элемент, относится к актиноидам, атомный номер 95. Стабильных изотопов не имеет. Синтезирован в конце 1944 - начале 1945 американскими учёны ...
Вискозиметрия
в разбавленных растворах полимеров
Полимеры, при их растворении в растворителе, значительно увеличивают
вязкость раствора. Полимеры используются в качестве сгустителей в таких
продуктах, как шампуни и мороженое. Этот эффект ...