Вольтамперометрия с линейной разверткой потенциалаМатериалы / Электроаналитические методы в аналитической химии / Вольтамперометрия с линейной разверткой потенциала
Термины вольтамперометрия и амперометрия относятся к методам, при которых на клеммы электродов электрохимической ячейки накладывается изменяющийся потенциал; при этом в ячейке имеются так называемые электроактивные (то есть способные к окислению или восстановлению) соединения, а проводимость внутри ячейки обеспечивается индифферентным, или поддерживающим, электролитом.
Ток через ячейку постоянно измеряется, в результате чего возникает кривая зависимости тока от наложенного потенциала, которую называют вольтамперограммой.
Наиболее простой вариант метода- это волътамперометрия с линейной разверткой потенциала. Типичная вольтамперограмма показана на рисунке.
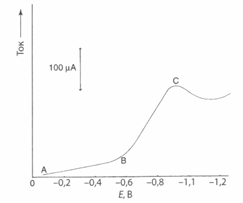
В начале кривой (точка А) ток небольшой. Между точками А и В очень медленный подъем кривой обусловлен остаточным (или примесным) током и зарядкой двойного слоя на границе электрода с раствором. Этот ток иногда называют фоновым. В точке В наложенный потенциал приближается к потенциалу восстановления частиц, находящихся в окисленном состоянии (Ох). При дальнейшем увеличении потенциала электроны с возрастающей скоростью переходят с электрода на Ох в соответствии со следующим уравнением реакции:
Все возрастающая скорость восстановления приводит к увеличению тока через ячейку. Можно показать, что общий ток через ячейку в этой области кривой слагается из катодного тока, или тока восстановления (г'с), и анодного тока.
По мере увеличения наложенного потенциала Е возрастает iс и падает ia, что и вызывает наблюдаемый подъем вольтамперометрической волны. Однако этот подъем не бесконечен: концентрация Ох в приэлектродном пространстве падает за счет его восстановления, а скорость Ох из раствора к электроду ограничена. В результате в точке С ток достигает своего пикового значения (рис. 2.9).
Влияние скорости диффузии Ох на величину диффузионного тока id определяется первым законом диффузии Фика, согласно которому:
Поток вещества к поверхности электрода = dN/dt = D dC/dx,
Второй закон диффузии Фика описывает уменьшение концентрации вещества в данной точке пространства во времени.
В приведенных выше уравнениях С — это концентрация вещества (например, Ox), N - его количество в молях, D — коэффициент диффузии, а х — расстояние от поверхности электрода.
Смотрите также
Уран
...
Методы определения хлорид-ионов
Защите окружающей среды от возрастающей антропогенной нагрузки в
настоящее время уделяется все большее внимание во всем мире. Развитие
промышленности, в том числе и химической, увеличение до ...
Механизм формирования вторичных месторождений меди и цинка
В
месторождениях рудных полезных ископаемых сосредоточена ничтожная часть общего
запаса элементов, большая часть элементов рассеяна в земной коре. Следовательно,
для образования месторожден ...
