Азотсодержащие
производные углеродаМатериалы / Химические соединения на основе кремния и углерода / Азотсодержащие
производные углерода
![]() Циановодородная (синильная) кислота HCN (H-C = N) - бесцветная легко подвижная жидкость, кипящая при 299,5 К. При 283 К она затвердевает. HCN и ее производные чрезвычайно ядовиты. HCN можно получить по реакции
Циановодородная (синильная) кислота HCN (H-C = N) - бесцветная легко подвижная жидкость, кипящая при 299,5 К. При 283 К она затвердевает. HCN и ее производные чрезвычайно ядовиты. HCN можно получить по реакции
![]()
В воде синильная кислота растворяется; при этом она слабо диссоциирует
HCN=H++CN-, К=6,2.10-10.
Соли синильной кислоты (цианиды) в некоторых реакциях напоминают хлориды. Например СН---ион с ионами Ag+ дает плохо растворимый в минеральных кислотах белый осадок цианида серебра AgCN. Цианиды щелочных и щелочноземельных металлов растворимы в воде. Из-за гидролиза их растворы пахнут синильной кислотой (запах горького миндаля). Цианиды тяжелых металлов плохо растворимы в воде. CN--сильный лиганд, важнейшими комплексными соединениями являются K4 [Fe (CN) 6] и Кз [Ре (СN) 6].
Цианиды - непрочные соединения, при длительном воздействии содержащегося в воздухе СO2 цианиды разлагаются
2KCN+C02+H20=K2C03+2HCN.
(CN) 2 - дициан (N=C-C=N) –
бесцветный ядовитый газ; с водой взаимодействует с образованием циановой (HOCN) и синильной (HCN) кислот:
(HCN) кислот:
(CN) 2+H20==HOCN+HCN.
В этой, как и в реакции, приведенной ниже, (CN) 2 похож на галоген:
СО+ (CN) 2=CO (CN) 2 (аналог фосгена).
Циановая кислота известна в двух таутомерных формах:
![]() H-N=C=O==H-0-C=N.
H-N=C=O==H-0-C=N.
Изомером является кислота H-0=N=C (гремучая кислота). Соли HONC взрывают (используются как детонаторы). Родановодородная кислота HSCN - бесцветная, маслянистая, летучая, легко затвердевающая (Тпл=278 К) жидкость. В чистом состоянии очень неустойчива, при ее разложении выделяется HCN. В отличие от синильной кислоты HSCN достаточно сильная кислота (К=0,14). Для HSCN характерно таутомерное равновесие:
H-N = С = S=H-S-C =N.
SCN - ион кроваво-красного цвета (реактив на ион Fe3+). Производные от HSCN соли-роданиды - легко получить из цианидов путем присоединения серы:
KCN+S=KSCN.
Большинство роданидов растворимо в воде. Нерастворимы в воде соли Hg, Au, Ag, Си. Ион SCN-, как и CN-, склонен давать комплексы типа Мз1 M" (SCN) 6, где M''Cu, Mg и некоторые другие. Диродан (SCN) 2-светло-желтые кристаллы, плавящиеся - 271 К. Получают (SCN) 2 по реакции
2AgSCN+Br2==2AgBr+ (SCN) 2.
Из других азотсодержащих соединений следует указать цианамид
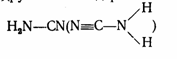
и его производное - цианамид кальция CaCN2 (Ca=N-C=N), который используется в качестве удобрения [4,464].
Смотрите также
Теория симметрии молекул
Понятие симметрии играет важную роль во всех естественных науках.
Свойствами симметрии обладают структуры многих молекул, ионов, образуемых ими
реагирующих систем.
Математической основой ...
Электроаналитические методы в аналитической химии
Одни
из наиболее сложных электрохимических методов – электроаналитические методы –
сегодня используются довольно часто, поскольку позволяют получить богатую
экспериментальную информацию о к ...
М.В.Ломоносов
Михаил Васильевич Ломоносов – русский
ученый-энциклопедист.
(1711-1765)
Сын крестьянина-помора, выходец из глухой деревушки
Архангельской губернии, Ломоносов с огром ...
