Структура молекулы воды и ее ионовМатериалы / Структура молекулы воды и ее ионовСтраница 5
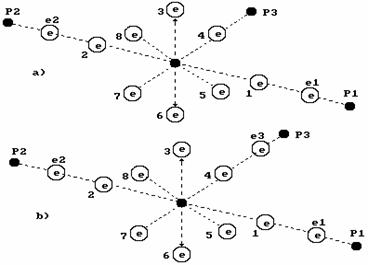
Рис. 6. Схема иона гидроксония ![]()
Чтобы один из кольцевых электронов вступил в связь с протоном или электроном соседнего атома, ему необходимо подняться в своей ячейке и удалиться от ядра атома кислорода. Для реализации такого процесса ему необходимо поглотить фотон из окружающей среды. Если это произойдет, то он удалится от ядра, приблизится к поверхности атома, и лишь тогда появятся условия для взаимодействия между электрическими и магнитными полями обоих электронов. Если один из кольцевых электронов атома кислорода соединится с электроном атома водорода, то образуется ион гидроксония ![]() , который и сформирует кислотные свойства воды (рис. 6).
, который и сформирует кислотные свойства воды (рис. 6).
При таком развитии событий на поверхности молекулы воды появятся три зоны с положительным потенциалом и она станет положительно заряженным ионом ![]()
![]() , который называют гидроксонием (рис. 4). Таким образом, кислотные свойства раствора определяет не протон (положительный ион
, который называют гидроксонием (рис. 4). Таким образом, кислотные свойства раствора определяет не протон (положительный ион ![]() ), а положительный ион гидроксония
), а положительный ион гидроксония ![]() . Процесс удаления электрона от ядра атома сопровождается поглощением фотонов из окружающей среды, поэтому процесс образования иона гидроксония эндотермический.
. Процесс удаления электрона от ядра атома сопровождается поглощением фотонов из окружающей среды, поэтому процесс образования иона гидроксония эндотермический.
Перекись водорода ![]() , также образуется из воды. В её структуре два атома кислорода
, также образуется из воды. В её структуре два атома кислорода ![]() и два атома водорода
и два атома водорода ![]() (рис. 7).
(рис. 7).
Чистая перекись водорода – бесцветная сиропообразная жидкость, обладающая сильными окислительными свойствами. Эта особенность перекиси водорода позволяет установить комбинации атомов кислорода и водорода, которые может иметь эта жидкость.
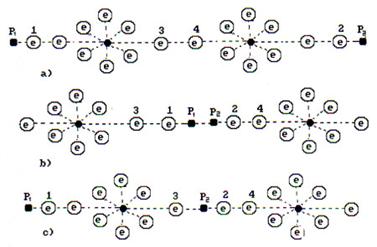
Рис. 7. Схемы молекул перекиси водорода ![]()
Варианты комбинации атомов водорода и кислорода представлены на рис. 7. Структура, представленная на рис. 7, а, эквивалентна молекуле воды (рис. 2), так как концы оси молекулы завершаются протонами (![]() и
и ![]() ) атомов водорода. Такая структура не может быть активной, так как активность определяют электроны. Поэтому есть основания полагать, что молекула перекиси водорода имеет структуру, показанную на рис. 7, b. У этой структуры на концах оси электроны, так же как и у молекулы кислорода.
) атомов водорода. Такая структура не может быть активной, так как активность определяют электроны. Поэтому есть основания полагать, что молекула перекиси водорода имеет структуру, показанную на рис. 7, b. У этой структуры на концах оси электроны, так же как и у молекулы кислорода.
Смотрите также
Производство серной кислоты
...
Фосфор (Phosphorus), Р
В темной комнате или ночью на улице попробуйте сделать такой простой опыт. Не очень сильно, так, чтобы не загорелась спичка, чиркните ею по спичечной коробке. Вы заметите, что некоторое время на терке ...
Бром (Bromum), Br
Бром - химический элемент VII группы периодической системы Менделеева, относится к галогенам; атомный номер 35, атомная масса 79,904; красно-бурая жидкость с сильным неприятным запахом. Б. откры ...
