Ароматические галогенпроизводные. Способы полученияМатериалы / Синтез нитрата 1-окси-3-адамантанкарбоновой кислоты / Ароматические галогенпроизводные. Способы получения
1. Прямое воздействие галогенов на ароматические углкводороды.
Галогены могут реагировать с ароматическим углеводородом тремя путями:
а) присоединяться к двойным связям бензольного кольца;
б) замещать водородный атом бензольного конца с образованием галогенарила;
в) замещать водородный атом в алкильной группе боковой цепи с образованием арилалкилгалогенида.
При действии на ароматические углеводороды галогенов (хлор, бром) на холоду в присутствии катализаторов происходит замещение водородных атомов в ядре с выделением гелагеноводородов:
FeCl3
C6H6 + Cl2 → C6H6Cl + HCl
Катализатором при этом обычно является хлорид или бромид железа (ІІІ). В качестве катализаторов могут быть также использованы хлориды других металлов, такие, как AlCl3, SbCl3, SbCl5, а также иод.
Роль катализатора заключается в активации (поляризации) галогена, который осуществляет электрофильное замещение в бензольном ядре. В присутствии FeCl3 хлорирование идет, например, по схеме:
FeCl3 + :Cl::Cl: ↔ FeCl-4 + Cl:+
۠۠۠ ۠ ۠۠۠۠۠ ۠ ۠ ۠۠
C6H6 + Cl+ → C6H5Cl + H+;
H+ + Cl2 → HCl + Cl+ и т. д.
В боковую цепь можно ввести галоген в отсутствии катализаторов на свету или при нагревании. Механизм замещения в этом случае радикальный. Для толуола эти превращения могут быть выражены схемой:
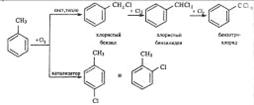
Галогены относятся к заместителям первого рода, и потому при галогенировании бензола второй атом галогена вступает преимущественно в n-положение к первому. Однако галогены в отличие от других заместителей первого рода затрудняют замещение (по сравнению с бензолом).
При хлорировании n-фторхлорбензола третий атом галогена вступает в о-положение к хлору, а не к фтору. Следовательно, решающее влияние на порядок замещения оказывает индукционный эффект галогена (о-положение к атому фтора имеет большой положительный заряд, так как –IF > -ICl):
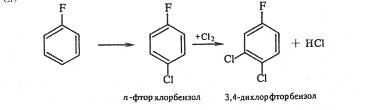
2.Замена аминогруппы галогеном через промежуточное образование диазосоединений. Этот способ позволяет получать любые галогенпроизводные, в том числе и фторпроизводные:
Cu2Cl2
───→ C6H5Cl + N2
HONO + HCl KI
C6H5NH2───→ C6H5N2Cl ────→ C6H5I + KCl +N2
Cu2Br2
───→ C6H5Br + Cu2Cl2 + N2
[C6H5N2]BF4 → C6H5F + N2 + BF3
Смотрите также
Стандартизация измерения рН в неводных средах. Методы определения рН стандартных буферных растворов
Данная курсовая
работа содержит 3 раздела, 35 страниц и 2 таблицы.
Целью работы
является изучение кислотности неводных растворов, методы ее определения и
стандартизация измерения, а такж ...
Получение гидроксида натрия
...
Плутоний (Plutonium), Pu
Изотоп плутония 238Pu впервые искусственно получен 23.02.1941 года группой американских ученых во главе с Г. Сиборгом путем облучения ядер урана дейтронами. Примечательно, что только после искусственн ...
