2. Уравнение изотермы химической реакцииКниги / Физическая химия / ЛЕКЦИЯ № 5. Химическое равновесие / 2. Уравнение изотермы химической реакции
Если реакция протекает обратимо, то ΔG = 0.
Если реакция протекает необратимо, то ΔG ≤ 0 и можно рассчитать изменение ΔG.
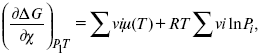
где χ – пробег реакции – величина, которая показывает, сколько молей изменилось в ходе реакции. I сп – характеризует равновесное и неравновесное состояние реакции, II сп – характеризует только неравновесные состояния.
Если
д χ = 1,
то
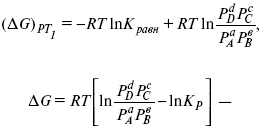
это уравнение изотермы химической реакции
.
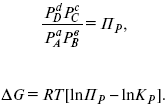
С помощью уравнения изотермы химической реакции можно судить о направлении протекания реакции.
1) Пp< Кp, ΔG < 0, слева направо;
2) Пp> Кp, ΔG > 0, справа налево;
3) Пp= Кp, ΔG = 0, химическое равновесие.
Смотрите также
Свинец (Plumbum), Pb
Свинец - металл, который, подобно меди, сурьме и олову, известен с глубокой древности.
Как ни странно, но впервые широкое применение свинец нашел там, где ныне он совершенно не употребляется, - при ...
Кремний
Коробецкая Анастасия 10А
класс
КРЕМНИЙ
Научный
руководитель: Сукачева Т.А.
Ядро: возможна большая доля силикатов
Земная
кора: глины, граниты, базальты, полевые шпаты.
...
Переработка жидкого топлива
К жидким химическим топливам относятся нефть и продукты ее
переработки (нефтепродукты), а также продукты гидрирования твердого топлива. В
настоящее время практическое значение имеют только н ...
