Ингибиторная защитаМатериалы / Методы защиты от коррозии металлов и сплавов / Ингибиторная защитаСтраница 2
Уменьшение содержания растворенного в коррозионной среде кислорода тормозит реакцию его восстановления, а следовательно, и скорость коррозии.
Перенапряжение водорода может быть повышено при введении в коррозионную среду солей некоторых тяжелых металлов — As Cl3, Bi2(SO4)3. Происходит контактное осаждение этих металлов, что затрудняет реакцию выделения водорода и тем самым - процесс коррозии, так как он протекает с водородной деполяризацией. На рис. 48 показано влияние небольшой добавки As2O3 (0.045% в пересчете на мышьяк) на скорость коррозии углеродистой стали в серной кислоте.
Сокращение площади катодов достигается добавлением экранирующих катодных ингибиторов, которые образуют на микрокатодах нерастворимые соединения, отлагающиеся в виде изолирующего защитного слоя. Для железа в водной среде такими соединениями могут быть Zn SO4, Zn CI2, а чаще Са(НСО3)2.
Бикарбонат кальция Са(НСО3)2 — самый дешевый катодный экранирующий ингибитор, применяемый для защиты стали в системах водоснабжения. Бикарбонат кальция в подщелоченной среде образует нерастворимые соединения СаСО3, осаждающиеся на поверхности, изолируя ее от электролита. Этим объясняется меньшая коррозия стали в жесткой воде по сравнению с умягченной.
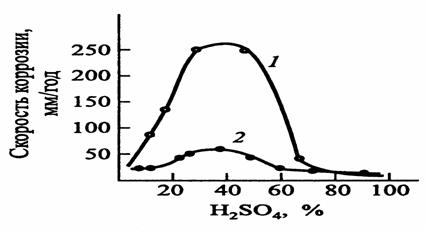
Рисунок - Зависимость скорости коррозии стали в растворах H2SO4:
1 – H2SO4; 2 – H2SO4 + As3+ (0,045%)
Катодные ингибиторы по защитному действию менее эффективны, чем анодные. Однако они совершенно безопасны, так как не вызывают усиления коррозии при их недостаточном содержании.
Анодные неорганические ингибиторы образуют на поверхности металла тонкие (~ 0,01 мкм) пленки, которые тормозят переход металла в раствор. К группе анодных замедлителей коррозии относятся химические соединения — пленкообразователи и окислители, часто называемые пассиваторами.
Катодно-анодные неорганические ингибиторы, например KJ, КВг в растворах кислот, тормозят в равной степени анодный и катодный процессы за счет образования на поверхности металла хемосорбционного слоя.
Пленкообразующие ингибиторы защищают металл, создавая на его поверхности фазовые или адсорбционные пленки. В их число входят некоторые соединения со щелочными свойствами: фосфаты; полифосфаты; силикаты; бораты и др.
Их ингибирующее действие проявляется только при наличии растворенного кислорода, который и играет роль пассиватора. Не являясь окислителями, эти вещества лишь способствуют адсорбции кислорода на поверхности металла. Кроме того, они тормозят анодный процесс растворения из-за образования защитных пленок, представляющих собой труднорастворимые продукты взаимодействия ингибитора с ионами переходящего в раствор металла. Так, например, фосфаты, адсорбируясь на поверхности стали, образуют с ионами железа экранирующие пленки, состоящие из смеси γ·Fe2О3 и FePO4·2H2O. Для большего защитного эффекта фосфаты часто используются в смеси с полифосфатами.
Чаще всего в качестве пассиваторов используют неорганические окислители: хроматы, нитриты, молибдаты, вольфраматы. Легко восстанавливаясь на катодных поверхностях, они ведут себя как деполяризаторы, вызывая появление на анодных участках плотностей тока, превышающих величины, необходимые для их пассивации. При этом стационарный потенциал облагораживается на несколько десятых вольта, а скорость анодного перехода в раствор ионов корродирующего металла резко снижается.
Пассиваторы тормозят анодную реакцию растворения металла благодаря образованию на его поверхности оксидов
Me + nН2О → Ме Оn + 2nН+ + 2nе
Эта реакция может протекать только на металлах, склонных к пассивации.
Смотрите также
Методика
проведенных экспериментов
Изучение процесса комплексообразования проводилось методом
рН-метрического титрования. Оно проводилось при помощи иономера с точностью
измерения ±0,05 ед. рН со стеклянным и хлорсеребряным электрода ...
Осмий (Osmium), Os
Попробуйте подсчитать, какой путь совершает кончик пера автоматической ручки при движении по бумаге только в пределах одной тетради в 12 листов. Пусть это будет зависеть от величины букв, манеры письм ...
