Реакции второго порядкаМатериалы / Коллоидная химия / Реакции второго порядка
Для реакций второго порядка кинетическое уравнение имеет следующий вид:
![]() (II.14)
(II.14)
либо
![]() (II.15)
(II.15)
Рассмотрим простейший случай, когда кинетическое уравнение имеет вид (II.14) или, что то же самое, в уравнении вида (II.15) концентрации исходных веществ одинаковы; уравнение (II.14) в этом случае можно переписать следующим образом:
![]() (II.16)
(II.16)
После разделения переменных и интегрирования получаем:
![]() (II.17)
(II.17)
Постоянную интегрирования g, как и в предыдущем случае, определим из начальных условий. Получим:
![]() (II.18)
(II.18)
Т.о., для реакций второго порядка, имеющих кинетическое уравнение вида (II.14), характерна линейная зависимость обратной концентрации от времени (рис. 2.4) и константа скорости равна тангенсу угла наклона прямой к оси времени:
![]() (II.19)
(II.19)
![]() (II.20)
(II.20)
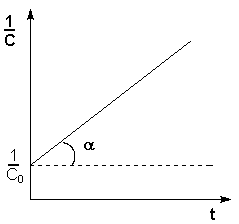
Рис. 2.4
Зависимость обратной концентрации от времени для реакций второго порядка
Если начальные концентрации реагирующих веществ Cо,А и Cо,В различны, то константу скорости реакции находят интегрированием уравнения (II.21), в котором CА и CВ – концентрации реагирующих веществ в момент времени t от начала реакции:
![]() (II.21)
(II.21)
В этом случае для константы скорости получаем выражение
![]() (II.22)
(II.22)
Порядок химической реакции есть формально-кинетическое понятие, физический смысл которого для элементарных (одностадийных) реакций заключается в следующем: порядок реакции равен числу одновременно изменяющихся концентраций. В случае элементарных реакций порядок реакции может быть равен сумме коэффициентов в стехиометрическом уравнении реакции; однако в общем случае порядок реакции определяется только из экспериментальных данных и зависит от условий проведения реакции. Рассмотрим в качестве примера элементарную реакцию гидролиза этилового эфира уксусной кислоты (этилацетата), кинетика которой изучается в лабораторном практикуме по физической химии:
СН3СООС2Н5 + Н2О ––> СН3СООН + С2Н5ОН
Если проводить эту реакцию при близких концентрациях этилацетата и воды, то общий порядок реакции равен двум и кинетическое уравнение имеет следующий вид:
![]() (II.23)
(II.23)
При проведении этой же реакции в условиях большого избытка одного из реагентов (воды или этилацетата) концентрация вещества, находящегося в избытке, практически не изменяется и может быть включена в константу скорости; кинетическое уравнение для двух возможных случаев принимает следующий вид:
1) Избыток воды:
![]() (II.24)
(II.24)
![]() (II.25)
(II.25)
2) Избыток этилацетата:
![]() (II.26)
(II.26)
![]() (II.27)
(II.27)
В этих случаях мы имеем дело с т.н. реакцией псевдопервого порядка. Проведение реакции при большом избытке одного из исходных веществ используется для определения частных порядков реакции.
Смотрите также
Индий (Indium), In
Индий - химический элемент III группы периодической системы Менделеева; атомный номер 49, атомная масса 114,82; белый блестящий мягкий металл. Элемент состоит из смеси двух изотопов: 113In (4,33%) и 1 ...
Химический элемент ванадий
В начале XIX в. в
Швеции были найдены новые богатые месторождения железной руды. Одна за другой
сооружались доменные печи. Но что примечательно: при одинаковых условиях
некоторые из ни ...
Степень набухания целлюлозы в растворах щелочей
При действии на целлюлозу растворов щелочей
происходят как структурные и химические ее изменения, так и физико-химические
процессы. Последние приводят к интенсивному набуханию целлюлозы и к ...
