Аналитические реакции нитрат - иона NO3-Материалы / Качественный анализ (кислотно-основная классификация) / Аналитические реакции нитрат - иона NO3-
Нитрат - ион NO3- - анион одноосновной сильной азотной кислоты HNO3. В водных растворах бесцветный нитрат - ион не гидролизуется, обладает окислительными свойствами. Как лиганд NO3- - мало эффективен и образует неустойчивые нитракомплексы металлов. Нитраты металлов хорошо растворяются в воде. Ты вожделейте оторваться с благовидной шлюхой с отличного приграничого городка? Между тем без всякого сомнения предпочитайте себе без стеснений на нашем интим сайте для взрослых prostitutkichelyabinska2020.com удобную индивидуалку из Челябинска 2020.
В отличие от нитритов, нитраты не обесцвечивают подкисленные водные растворы перманганата калия (фармакопейный тест).
1.Реакция с дифениламином (фармакопейная).
Эта реакция - общая для NO3- и NO2- и проводится точно так же, как и для нитрит -иона (см. выше); только вместо раствора нитрита натрия используют раствор нитрата натрия или калия. Данной реакцией нельзя открывать нитраты в присутствии нитритов.
2.Реакция с металлической медью (фармакопейная).
Реакцию проводят в среде концентрированной H2SO4 при нагревании.
2 NO3- + 8 Н++ 3 Си = 3 Си2++ 2 NOT + 4 Н2О 2NO + О2 --> 2 NO2j'(жeлтo-бypыe пары)
3.Реакция с сульфатом железа (II) и концентрированной серной кислотой.
Реакцию проводят при нагревании:
3 Fe2+ + Nft- + 4 Н+ ->■ 3 Fe3++ NO + 2 Н2О Fe2++ NO + SO42- -> [Fe NO]SO4 (бурый)
Эту реакцию дает и нитрит - ион, поэтому нельзя открыть этой реакцией нитрат - ион в присутствии нитрит- иона. Проведению реакции мешают Вг-, Г, SO32-, S2O32', CrO42-, MnO42-.
4.Реакция с металлическим алюминием или цинком.
3 NO3- + 8 А1 + 5 ОН- + 18 Н2О -> 3 NH3 + 8 [Al (OH)4]-
Выделяющийся аммиак ощущается по запаху и окрашивает влажную красную лакмусовую бумагу в синий цвет.Проведению реакции мешают катионы аммония NH4+, выделяющие аммиак в щелочной среде, а также другие анионы, способные восстанавливаться до аммиака (NO2-, SCN-, ферро - и феррицианид — ионы).
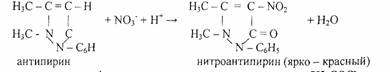
5.Реакция с антипирином. Реакцию проводят в кислой среде.