Аналитические реакции катиона меди (II) Си2+.Материалы / Качественный анализ (кислотно-основная классификация) / Аналитические реакции катиона меди (II) Си2+.
Акво - ионы меди (II) [Си(Н2О)п]2+ окрашены в голубой цвет, поэтому растворы солей меди (II) имеют голубую окраску с разными оттенками (от голубой до сине-зеленой). В водных растворах акво - ионы меди (II) частично гидролизуются с образованием растворимых гидроксо-аквокомплексов состава [Cu(H2O)n.m(OH)m]2-m по схеме:
[Cu(H2O)]2+ + mH2O = [Cu(H2O)n.m(OH)m] m + тН3О+
1.Реакция с щелочами.
Си2++ 2 ОН-— Си(ОН)2 (сине-зеленый)
Смесь осторожно нагревают до кипения и кипятят до потемнения осадка. Си(ОН)2 разлагается, теряя воду и образуется черный осадок оксида меди (II) СuО: Сu (ОН)2 — СuО (черный) + Н2О
Осадок Сu (ОН)2 растворяется в кислотах, в растворах аммиака (с образованием комплекса [Cu(NH3)4] + синего цвета), комплексообразующих органических кислот (лимонная, винная), частично растворим в концентрированных щелочах с образованием гидроксокомплексов меди (II).
2.Реакция с аммиаком (фармакопейная).
СuСЬ + NHrH2O — Си(ОН)С1 |(сине-зеленый) В избытке аммиака осадок растворяется с образованием ярко синего раствора:
Сu (ОН)С1 + 4 NH3-H2O — [Cu(NH3)4]2+ + ОН- + СГ + 4 Н2О В кислой среде комплексный тетрамминмедь (II) - катион разрушается:
[Си(Ш3)4]2+(ярко - синий) + 4 Н3О+ — [Сu (Н2О)4]2+(голубой) + 4 NH4+ и окраска раствора из ярко-синей переходит в голубую (цвет аквокомплекса меди (II)). К аммиачному комплексу меди (II) прибавляют по каплям разбавленный раствор одной из кислот - НС1, HNO3 или H2SO4. Окраска раствора из ярко - синей переходит в голубую. Мешают катионы Со2+, Ni2+, олово (II).
3.Реакция с гексацианоферратом (II) калия.
2Cu2+ + [Fe(CN)6]4- — Си2[Ре(СЫ)6]|(красно-коричневый).
Капельный метод на фильтровальной бумаге: на лист фильтровальной бумаги, пропитанной раствором ферроцианида калия, наносят каплю раствора соли меди (II). На бумаге образуется красно-коричневое пятно.
Осадок не растворяется в разбавленных кислотах, но растворяется в 25%-м водном аммиаке:
Cu,[Fe(CN)6] + 12 NH3+ 4 Н2О — ( NH4)4[Fe(CN)6] + 2 [Cu(NH3)4](OH)2 Проведению реакции мешают катионы, также образующие окрашенные осадки .и ферроцианидов (Fe3+, Со2т, Ni2+).
4.Реакция с тиосульфатом натрия.
2Си2+ + 2 82О32Хиз6ыток) + 2 Н2О — Cu2S |(темно-бурый) + §j +4 H++~2SO42~
Выпадает темный осадок, содержащий смесь Cu:S и S.
5. Реакция с купроном (1-бензоиноксимом).
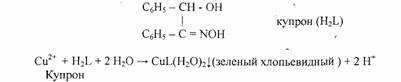
Реакцию проводят в аммиачной среде. Осадок не растворяется в избытке аммиака.
6. Реакция восстановления меди (II) металлами до металлической меди (фармакопейная).Реакцию дают металлы, расположенные в ряду напряжений металлов левее меди.
Cu2+ + Zn -- Си + Zn2+
Си2+ + Fe -> Си + Fe2+
3 Си2+ +2 А1 -► 3 Си +2 А13+
8. Соли меди окрашивают пламя газовой горелки в изумрудно-зеленый цвет. Реакция с тиоцианат - ионами.
Си2+ + 2 SCN- — Cu(SCN)2J-+ CuSCN| + SCN- Образуется
черный осадок Cu(SCN)2, постепенно переходящий в белый CuSCN.
Другие реакции меди (II).
Катионы Си + с сульфид -ионами дают черный осадок сульфида меди CuS; с фосфатами
- голубой осадок Си3(РО4)2. Известны реакции комплексообразования меди (II) с различными органическими реагентами - купроином, купфероном, дитиоксамидом и др.
Смотрите также
Химия воды и микробиология
...
Медь и её свойства
МЕДЬ (лат. Cuprum), Cu (читается
«купрум»), химический элемент I группы периодической системы Менделеева,
атомный номер 29, атомная масса 63,546.
...
ИСТОРИЯ ФУЛКАНЕЛЛИ
Увы, увы, сын мой, наступит день, когда священные иероглифы превратятся в простых
идолов. Мир ошибочно примет знаки науки за богов и обвинит Древний Египет в поклонении
адским чудищам. Но те, кто ...
