Некоторые аспекты поиска, создания и изучения объектов ионики твердого
тела на примере работ, выполненных в Институте кристаллографии РАНМатериалы / Исследование твердых электролитов / Некоторые аспекты поиска, создания и изучения объектов ионики твердого
тела на примере работ, выполненных в Институте кристаллографии РАНСтраница 1
Целенаправленные исследования в этой области были начаты в 1980 г. Ионная проводимость твердых электролитов обеспечивается переносом самых различных ионов - одно-, двух-, трехзарядных катионов (Ag+, Cu+, Li+, Na+, K+, Rb+, Tl+, Cs+, Ca2+, Zn2+, Mg2+, Pb2+, Al3+, Sc3+, Ce3+, Eu3+) и анионов (F–, Cl–, Br–, O2–, S2–). Существуют материалы, где носителями заряда служат ионы двух или даже трех сортов, и вещества со смешанной ионно-электронной проводимостью. Особый интерес представляют суперионные проводники с Li+- и Na+- ионной проводимостью, поскольку именно они дают максимальный выигрыш в энергии, что гарантирует им будущее в производстве миниатюрных литиевых батареек и тяговых аккумуляторов для электромобилей. Поэтому все стремятся улучшить характеристики известных соединений или найти для этих ионов принципиально новые проводящие матрицы. Целенаправленное изменение характеристик соединений возможно только в случае, если нам удастся заглянуть в глубь кристалла, чтобы узнать, как и насколько эффективно способны перемещаться ионы в кристаллической решетке. Иначе говоря, нужно оценить потенциальные каналы проводимости и найти способы увеличения скорости движения заряженных частиц по ним. Рассмотрим в этом плане как достаточно известное соединение - ортофосфат лития Li3PO4, так и сравнительно новое - литий-замещенный титанат лантана La2/3-xLi3x}1/3–2xTiO3 ( - вакансия в позиции крупного катиона).
С середины 70-х годов ортофосфат лития известен как ионный проводник, в структуре которого пустоты кристаллического каркаса формируют сквозные прямые каналы вдоль осей а и с и зигзагообразные вдоль оси b (рис.3). Однако величина электропроводности не очень высока, поскольку, несмотря на "рыхлость" структуры, все катионы лития участвуют в постройке жесткого каркаса и не способны свободно перемещаться по каналам. Решение задачи увеличения ионной проводимости напрашивается само собой: необходимо поместить в каналы дополнительные катионы Li. Это достигается специальным введением в базовый материал гетеровалентных примесей, что и наблюдается в твердых растворах со структурой высокотемпературной модификации Li3PO4.
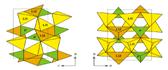
Рис.3. Каналы проводимости в структуре Li3PO4 образуются при формировании каркаса из связанных общими вершинами тетраэдров [Li1O4], [Li2O4] и [PO4]. а - проекция bc, б - проекция аb.
Получаемые нестехиометрические фазы систем Li4GeO4-Li3VO4 и Li4GeO4-Li3PO4 обладают ионной проводимостью, значения которой составляют 10–4-10–5 Ом–1·см–1 уже при комнатной температуре. Чтобы понять механизм ионного транспорта, потребовалось провести экспериментальные исследования на монокристаллах больших размеров и хорошего качества. Монокристаллы Li3+xP1–xGexO4 (x=0.34) были выращены в Институте кристаллографии методом кристаллизации из раствора в расплаве. Величины удельной проводимости кристалла Li3.34P0.66Ge0.34O4 составляют 1.8·10–6 и 3.7·10–2 Ом–1·см–1 при 40° и 400°С соответственно - что, как видно из рис.4, на несколько порядков выше проводимости номинально чистого -Li3PO4.
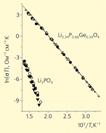
Рис.4. Ионная проводимость монокристаллов Li3PO4 и Li3+xP1–xGexO4. Разными значками изображены величины проводимости в различных кристаллографических направлениях.
Миграция ионов лития в твердом растворе Li3+xP1–xGexO4 связана с внедрением дополнительных катионов Li+ в пустоты кристаллического каркаса, что приводит к разупорядочению литиевой подрешетки не только в каналах проводимости, но и в жестком каркасе (рис.5), и число доступных для миграции лития позиций существенно возрастает. Кристаллическая структура при этом становится приблизительно одинаково "прозрачной" для ионного транспорта во всех направлениях, благодаря чему значения проводимости по трем главным кристаллографическим направлениям почти выравниваются (анизотропия проводимости в твердом растворе Li3+xP1–xGexO4 по сравнению с Li3PO4 понижается).
Смотрите также
Композиционные хемосорбционные волокнистые материалы "Поликон К", наполненные углеродными волокнами
Развитие
промышленности, успехи химии в области органического синтеза привели к тому,
что перед человечеством остро встала проблема охраны окружающей среды и ее
защиты от последствий собств ...
Химический элемент хром
Элемент №24. Один из самых
твердых металлов. Обладает высокой химической стойкостью. Один из важнейших
металлов, используемых в производстве легированных сталей. Большинство
соединений хром ...
Теория Бутлерова
...
