Химическая
модификация электродов с помощью ТПЭМатериалы / Исследование твердых электролитов / Химическая
модификация электродов с помощью ТПЭСтраница 1
Суть химической модификации электродов, сравнительно нового направления электрохимии, можно пояснить на следующем примере. Предположим, что необходимо провести реакцию электрохимического восстановления вещества Ox: Ox + e – → Red. Однако данная реакция на известных электродных материалах (реальный выбор которых, кстати, невелик) протекает с низкой скоростью. Выход известен — подбор катализатора, повышающего скорость реакции и иммобилизация его в реакционной зоне, то есть на границе раздела электрод/электролит. Собственно, одной из основных задач химической модификации электродных поверхностей и является организация эффективного протекания электрохимических процессов с помощью катализаторов, находящихся в модифицирующем слое.
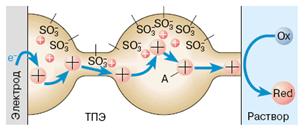
Рис. 5. Схема химически модифицированного электрода с ТПЭ и внедрённым в него электроактивным веществом А.
Предположим далее, что такой катализатор найден — некое вещество А (рис. 5). Нанесём слой ТПЭ на поверхность электрода и методом ионного обмена внедрим в него катализатор, заместив часть катионов натрия, находящихся в мембране. В этом случае реакция восстановления вещества Ox будет протекать не на поверхности электрода, а на границе раздела ТПЭ/раствор: Ox + A → Red + A +. Катализатор возвращается в исходную форму, восстанавливаясь на электроде: А + + е – → A. Однако для этого катион А + должен переместиться через слой полимера к электроду и, восстановившись, вернуться обратно к границе раздела полимер/раствор.
Механизм переноса заряженных частиц или просто заряда через слой полимера является ключевым вопросом, определяющим функционирование химически модифицированных электродов. Скорость переноса заряда часто определяет скорость электрохимических и каталитических процессов с участием ХМЭ, именно поэтому процессы переноса заряда в полимерах были и являются предметом многочисленных исследований.
В рассматриваемом примере катион А+ может достичь поверхности электрода по двум механизмам, первым из которых является физическая диффузия. Движущей силой диффузии является градиент концентрации А+ в ТПЭ в направлении, перпендикулярном поверхности электрода. Этот градиент возникает вследствие уменьшения концентрации А+ у поверхности электрода из-за электрохимического восстановления ЭАВ. Однако физическая диффузия практически всех катионов (за исключением H + и Na +) в ТПЭ "Nafion" протекает медленно, скорость движения резко падает с увеличением размера и заряда ионов. Скорость диффузии комплексных катионов в "Nafion" обычно характеризуется низкими коэффициентами диффузии в диапазоне 10–11 —10–13 см 2/с. Низкая скорость транспорта заряда делает малоэффективным и весь процесс на ХМЭ в целом.
Альтернативным механизмом, позволяющим А+ из глубины мембраны "достичь" поверхности электрода, является обмен электроном между близлежащими молекулами вещества А: A+ + А → А + A+. Восстановившись на электроде, ближайшая к нему молекула восстанавливает соседнюю и т. д. до границы раздела полимер/раствор. Разумеется, это возможно только в том случае, если расстояние между молекулами А в ТПЭ достаточно мало для переноса электрона, то есть концентрация А достаточно велика.
Относительный вклад переноса электрона (электронной проводимости) и диффузии в общий процесс переноса заряда в электрохимических системах, содержащих растворы электролитов, был рассмотрен Дамсом (H. Dahms) и Раффом (I. Ruff) в конце 70-х — начале 80-х годов. Аналогичная теоретическая модель переноса заряда была несколько позднее развита и для ТПЭ. Скорость процесса переноса заряда в рамках рассматриваемой модели может быть выражена через коэффициент диффузии заряда Dct , состоящий из двух слагаемых:
Dct = D + kδ 2 πCA/4,где D — коэффициент реальной диффузии вещества А в полимере, k — константа скорости процесса обмена электроном, л·моль –1 ·с –1,СА — концентрация вещества А в полимере, δ — расстояние между редокс-центрами, на которое переносится электрон.
Относительный вклад обеих составляющих транспорта заряда можно показать на следующих примерах. Так, в растворах электролитов при СА = 0,1М, δ = 10 –7 см, k = 10 9 см 3 ·моль –1 ·с –1 вклад электронного переноса составляет 8·10 –9 см 2 ·с –1. Эта величина значительно меньше коэффициентов физической диффузии веществ, обычно наблюдаемых в водных растворах ~10 –6 см 2 ·с –1. Иначе говоря, вклад электронного переноса в общий процесс переноса заряда в водных растворах незначителен. Дело обстоит иначе в ТПЭ, где физическая диффузия веществ, естественно, протекает с меньшей скоростью. Так, в системе, состоящей из комплекса [Ru(bipy)3] 2+ введённого в ТПЭ "Nafion", коэффициент диффузии заряда Dct, равный 4·10 –10 см 2 ·с –1, складывается из величин 0,3·10 –10 см 2 ·с –1 и 3,7·10 –10 см 2 ·с –1, отражающих соответственно физическое движение комплекса в полимере и электронный перенос заряда. Таким образом, в полимерных электродах для повышения эффективности протекающих на них процессов необходимо стремиться к организации наряду с диффузионным и электронного переноса заряженных частиц через полимер.
Смотрите также
Коррозия меди в 5М изопропанольных растворах НС1
...
Индий (Indium), In
Индий - химический элемент III группы периодической системы Менделеева; атомный номер 49, атомная масса 114,82; белый блестящий мягкий металл. Элемент состоит из смеси двух изотопов: 113In (4,33%) и 1 ...
Крашение натурального шелка активными бромакриламидными ланазолевыми красителями
...
