Исследование эффективности разработанных ингибиторов
электрохимическими и гравиметрическим методамиМатериалы / Ингибиторы коррозии стали на основе фосфорсодержащих соединений и полиэлектролитов / Исследование эффективности разработанных ингибиторов
электрохимическими и гравиметрическим методамиСтраница 1
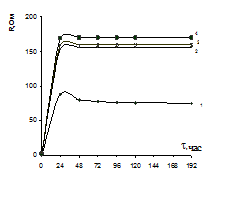
Ингибирование поверхности металла на катодных и анодных участках подразумевает существование определенной разности потенциалов между ними и, следовательно, протекание электрического тока. Этот ток, называемый коррозионным, эквивалентен количеству прокорродировавшего металла. В процессе коррозии потенциалы катодных и анодных участков не остаются постоянными, наблюдается поляризация, следствием которой является сближение потенциалов катода и анода и уменьшение коррозионного тока. Исследование антикоррозионных свойств ингибиторов заключается в экспериментальном изучении поляризационного сопротивления стального электрода или зонда в растворе фона и в присутствии различных ингибиторов. Все экспериментальные данные получены с использованием в качестве фона 3% ного раствора Na2SO4. На рис.1 (а, б), в качестве примера, приведены результаты измерений поляризационного сопротивления стального зонда в слабокислых средах, а также в присутствии ингибиторов: растворов полифосфата натрия, пирофосфата кальция, полиэлектролитов, а также двухкомпонентных ингибиторов полифосфат-унифлок, полифосфат-NaКМЦ, пирофосфат-NaКМЦ, пирофосфат-желатин. Из рис.1 видно, что введение в фоновый раствор индивидуальных ингибиторов увеличивает поляризационное сопротивление, а при введении двухкомпонентных смешанных ингибиторов наблюдается еще большее увеличение поляризационного сопротивления стального зонда. Такой результат указывает на резкое торможение электрохимического процесса и позволяет получить предварительные результаты об эффективности тех или иных ингибиторов.
А Б
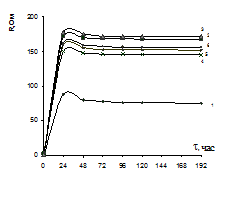
Рис. 1. Кривые поляризационного сопротивления стального электрода. В фоновом растворе (1); в присутствии 0,001% растворов ингибиторов: (NaPO3) n- NaКМЦ (2); (NaPO3) n- желатин (3); (NaPO3) n - унифлок (4) (а) и Са2Р2О7 - желатин (2); Са2Р2О7 - NaКМЦ (3); Са2Р2О7 (4); NaКМЦ (5); Желатин (6) (б).
На рис.2 (а, б) приведены результаты исследования кинетики электродных процессов и поляризационных измерений процесса коррозии стального электрода при различных температурах, а также в присутствии двухкомпонентных ингибиторов полифосфат натрия-унифлок и полифосфат натрия-желатин, из которого видно, что величина стационарного потенциала коррозии Ест. постоянна относительно нормального хлорсеребряного электрода в фоновом растворе и составляет - 0,670 В при температуре 20 0С. При добавлении к нему желатина значение потенциала коррозии увеличивается до - 0,490 В, наблюдается смещение поляризационных кривых на 180 мВ (рис.2 а), а при добавления унифлока на 190 мВ (рис.2 б) в сторону более положительных значений, характеризуя преимущественно торможение скорости анодной реакции. Одновременно с изменением потенциала коррозии наблюдается уменьшение тока коррозии, что указывает на смешанный механизм действия ингибитора.
Результаты расчетов значений стационарного потенциала (Ест) и тока коррозии (![]() ), коэффициента торможения (g), степени защиты (Z) и относительного стандартного отклонения при различных температурах приведены в таблице 1. Как видно из таблицы, растворы ингибиторов (NaPO3) n- унифлок при эквимолярном соотношении компонентов, при всех изученных температурах эффективны и принимают значения степени защиты от 91,40 до 95,16%. Присутствие смешанного ингибитора (NaPO3) n- NaКМЦ оказывает значительно меньшее действие на процесс электрохимической коррозии. Так, если при 200С степень защиты данного смешанного ингибитора равна 76,80%, то с повышением температуры защитный эффект незначительно изменяется и при достижении 800С снижается до 68,93% (табл.1).
), коэффициента торможения (g), степени защиты (Z) и относительного стандартного отклонения при различных температурах приведены в таблице 1. Как видно из таблицы, растворы ингибиторов (NaPO3) n- унифлок при эквимолярном соотношении компонентов, при всех изученных температурах эффективны и принимают значения степени защиты от 91,40 до 95,16%. Присутствие смешанного ингибитора (NaPO3) n- NaКМЦ оказывает значительно меньшее действие на процесс электрохимической коррозии. Так, если при 200С степень защиты данного смешанного ингибитора равна 76,80%, то с повышением температуры защитный эффект незначительно изменяется и при достижении 800С снижается до 68,93% (табл.1).
Отметим, что само по себе повышение величины скорости коррозии с ростом температуры не может служить доказательством того, что в ходе эксперимента увеличивалась доля активной поверхности металла. Достаточно высокие скорости коррозии могут наблюдаться в некоторых случаях и из пассивного состояния. Между тем, информация о состоянии поверхности стали в ходе коррозионных испытаний очень важна, так как
|
а |
б |
Смотрите также
Производство азотной кислоты
Азотная кислота является одной из важнейших минеральных
кислот и по объему производства занимает второе место после серной кислоты. Она
образует растворимые в воде соли (нитраты), обладает н ...
Кальцинация гидрокарбоната
...
Тест-системы для индикации ионов тяжёлых металлов в объектах окружающей среды
...


