Седиментация и диффузия. Гипсометрический закон.
Седиментационно-диффузионное равновесие. Скорость седиментацииСтатьи / Устойчивость дисперсных систем, седиментация и диффузия / Седиментация и диффузия. Гипсометрический закон.
Седиментационно-диффузионное равновесие. Скорость седиментацииСтраница 2
3. ![]() , т.е.
, т.е. ![]() ,
,
т.е. ![]()
![]()
В системе имеет место седиментационно-диффузионное равновесие.
Проинтегрируем это уравнение, разделив переменные:
![]()
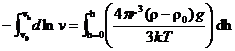 ;
;
Примем ![]() ,
,
![]() ,
,![]()
где vo – концентрация частиц на дне сосуда;
vh – концентрация частиц на высоте h от дна.
Отсюда 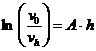
![]()
![]() - гипсометрический закон Лапласа-Перрена.
- гипсометрический закон Лапласа-Перрена.
В этом случае система является седиментационно-устойчивой, но распределение частиц в ней не равномерное, а равновесное
. Это распределение наблюдается, когда 10-5 < r < 10-3 см.
Если сравнить седиментацию с учетом диффузии и без нее, то видно различие факторов обусловливающих кинетическую устойчивость. Эти факторы позволяют различать кинетическую седиментационную устойчивость (КСУ) и термодинамическое равновесие, которого не может быть при КСУ. Мерой КСУ является величина, обратная константе седиментации.
![]()
Эта устойчивость обеспечивается гидродинамическими факторами: вязкостью и плотностью среды, плотностью и размерами частиц. КСУ измеряется в обратных сведбергах: обр. св. = 1013 с– 1.
ТСУ обусловлена статистическими законами диффузии и непосредственно связана с диффузионно–седиментазионным равновесием. Мерой ТСУ является гипсометрическая высота. Ее удобнее определять как высоту hе, на протяжении которой концентрация дисперсной фазы изменяется в e раз.
![]()
Из формулы следует, что hе и ТСУ тем больше, чем меньше размер частиц и разность между плотностями. Вязкость не влияет на ТСУ, а увеличение Т способствует повышению устойчивости, т.к. увеличивается тепловое движение. КСУ с увеличением Т убывает, за счет снижения вязкости среды.
Итак, седиментационная устойчивость дисперсных систем определяется, главным образом, размерами частиц дисперсной фазы:
· лиофобные золи (10– 7 – 10– 5 см) – седиментационно устойчивые системы, характерна диффузия, обеспечивающая равномерное распределение частиц по объему системы;
· микрогетерогенные системы (10– 5 10– 3 см) – устанавливается седиментационно – диффузионное равновесие, для которого характерно гипсометрическое распределение частиц по объему системы;
· грубодисперсные (более 10– 3 см) - седиментационно неустойчивые системы, происходит быстрая седиментация.
Зависимость распределения частиц по высоте в равновесном состоянии аналогична барометрической формуле Ла-Пласса для газов в атмосфере:
![]() ,
,
где m – масса частицы;
h1, h2 – высоты уровней замера;
с1, с2 – концентрации на уровнях h1 и h2 соответственно;
- плотность частицы;
0 - плотность среды.
При коагуляции золя смесью двух и более электролитов возможны три случая (рис. 3.1.2.3). По оси абсцисс отложена концентрация первого электролита С1, а Cк1 – его порог коагуляции. Аналогично по оси ординат отложена концентрация второго электролита С2, а Ск2 – его порог коагуляции.
1. Аддитивное действие электролитов (линия 1 рис. 3.1.2.3). Электролиты действуют как бы независимо один от другого, их суммарное действие складывается из воздействий каждого из электролитов. Если с1´ - концентрация первого электролита, то для коагуляции золя концентрация второго электролита должна быть равной с2´. Аддитивность наблюдается обычно при сходстве коагулирующей способности обоих электролитов.
2. Синергизм действия (линия 2 рис. 3.1.2.3). Электролиты как бы способствуют друг другу – для коагуляции их требуется меньше, чем нужно по правилу аддитивности (с2″ < c2′). Условия, при которых наблюдается синергизм, сформулировать трудно.
3. Антагонизм действия (линия 3 рис. 3.1.2.3). Электролиты как бы противодействуют друг другу и для коагуляции их следует добавить больше, чем требуется по правилу аддитивности. Антагонизм наблюдается при большом различии в коагулирующем действии электролитов.
Существует несколько теорий, объясняющих явление антагонизма. Одной из его причин может служить химическое взаимодействие между ионами.
Например, для золя AgCl, стабилизированного хлоридом калия, коагулирующем действием обладают катионы. Например, большой коагулирующей способностью обладает четырёхзарядный ион тория Th4+. Однако если взять для коагуляции смесь Th(NO3)4 и K2SO4, то коагулирующая способность этой смеси значительно меньше, чем отдельно взятого Th(NO3)4. Связано это с тем, что в результате химической реакции образуется комплекс:
Смотрите также
Ингибиторы коррозии стали на основе фосфорсодержащих соединений и полиэлектролитов
...
Получение неорганических веществ
...
Твердофазный синтез перрената калия
В настоящий момент большой интерес
представляет уже не столько изучение свойств веществ, в которые специально были
введены какие-то добавки (иногда это очень сильно меняет свойства исходного ...
