Уникальные свойства аммиака и его соединенийСтатьи / Уникальные свойства аммиака и его соединенийСтраница 1
По значимости в неорганической химической индустрии и неорганической химии аммиак - самое важное водородное соединение азота. При обычных условиях аммиак - бесцветный газ с резким запахом и едким вкусом. Он токсичен: раздражает слизистые оболочки, а острое отравление вызывает поражение глаз и воспаление легких. При охлаждении до -33,35˚С аммиак сжижается, превращаясь в бесцветную жидкость, а при -77,7˚С затвердевает (при н.у.).
По своей химической природе он представляет собой нитрид водорода H3N. В химическом строении аммиака sp3-гибридные орбитали атома азота образуют три связи с тремя атомами водорода, которые занимают три вершины чуть искаженного тетраэдра. Электроны связей Н-N довольно сильно смещены от водорода к азоту (азот более электроотрицателен, чем водород), поэтому молекула аммиака в целом характеризуется значительной полярностью.
Четвертая вершина тетраэдра занята неподеленной электронной парой азота, что дополнительно увеличивает полярность молекулы аммиака и обеспечивает химическую ненасыщенность и реакционноспособность его молекул.
В аммиаке между молекулами действуют водородные связи, вследствие чего аммиак обладает рядом экстремальных свойств по сравнению с другими водородными соединениями элементов пятой группы главной подгруппы. Вследствие полярности молекул и достаточно высокой диэлектрической проницаемости жидкий аммиак является хорошим неводным растворителем. В жидком аммиаке хорошо растворяются щелочные и щелочно-земельные металлы, сера, фосфор, йод, многие соли и кислоты. Вещества с функциональными полярными группами в жидком аммиаке подвергаются электролитической диссоциации.
По растворимости в воде аммиак превосходит любой другой газ: при 0˚С 1 объем воды поглощает 1200 объемов газообразного аммиака. Прекрасная растворимость аммиака в воде обусловлена возникновением межмолекулярных водородных связей.
Интересным свойством молекул аммиака является их способность к структурной инверсии, т.е. к "выворачиванию наизнанку" путём прохождения атома азота сквозь образованную атомами водорода плоскость основания пирамиды. Потенциальный барьер этой инверсии равен 25 кДж/моль, осуществлять её могут лишь молекулы, достаточно богатые энергией. Скорость инверсии сравнительно невелика - она в 1000 раз меньше скорости ориентации молекул NH3 электрическим полем. С такой инверсией связано электромагнитное излучение строго определённой частоты в радиодиапазоне СВЧ. На молекулах NH3 советские физики в 1955 году создали новый вид генератора излучения – так называемый мазер.
Аммиачный мазер позволил создать аппаратуру для очень точного измерения времени. Благодаря таким сверхточным «молекулярным часам» установлено, что продолжительность земных суток ежегодно возрастает в - среднем на 0,00043 секунд.
Химические свойства. Аммиак весьма реакционноспособное соединение. Благодаря неподелённой электронной паре у атома N для NH3 особенно характерны и легко осуществимы реакции присоединения. Партнёрами аммиака в таких реакциях могут быть молекулы и ионы, способные предоставить для электронной пары азота место на своих незаполненных электронных оболочках. Типичный пример — образование иона аммония путём присоединения иона водорода Н+ к молекуле NH3
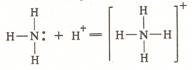
Или в другой записи:
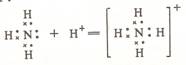
В ионе аммония все связи ковалентны и неразличимы (равноценны). Такой механизм образования химической ковалентной связи называют донорно-акцепторным, а связь — координационной. Атом азота, имеющий свободную электронную пару,— донор; ион водорода Н+, предоставляющий место этой паре на свободной электронной оболочке,— акцептор. Со многими солями аммиак образует продукты присоединения — аммиакаты (например, CuSO4*5NH3, CuSO4*4NH3*H2O). Они подобны гидратам.
По поводу растворения А. в воде существовало мнение, что это — химическое взаимодействие по схеме:
Смотрите также
Криптон (Kryptonum), Kr
Находится в атмосферном воздухе. Образуется при ядерном делении, в том числе и в результате естественных процессов, происходящих в рудах радиоактивных металлов.
Производство сверхмощных эксимерных лаз ...
Курс лекций по Коллоидной химии (Часть 1)
...
Изотермы адсорбции паров летучих органических веществ на пористых углеродных материалах
Антропогенные
изменения окружающей среды становятся все более значимыми по мере усиления
хозяйственной деятельности человека. Научно – технический прогресс ведет к
заметным, иногда непредск ...
