ТеплоемкостьСтатьи / Теплоемкость органических веществ и ее прогнозирование методом Бенсона и при повышенном давлении / ТеплоемкостьСтраница 1
Теплоемкость есть свойство вещества, характеризующее отношение количества тепла, сообщенного этому веществу, к вызванному им изменению температуры. Согласно более строгому определению, теплоемкость - термодинамическая величина, определяемая выражением
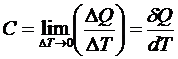 , (3.1)
, (3.1)
где ![]() - количество теплоты, сообщенное системе и вызвавшее изменение ее температуры на
- количество теплоты, сообщенное системе и вызвавшее изменение ее температуры на ![]() .
.
Знание теплоемкости необходимо для выполнения самых разнообразных расчетов, например, при расчете тепловых балансов, при проектировании всевозможной теплообменной аппаратуры и реакторов, при расчете химического равновесия и пр. Знание температурной зависимости теплоемкости необходимо при определении энтропии вещества, изучение теплоемкости вещества несет важную информацию о строении его молекул и пр.
При практических расчетах используются следующие понятия:
· средняя теплоемкость - это отношение конечных разностей ![]() ;
;
· истинная теплоемкость - это отношение бесконечно малых величин ![]() ;
;
· теплоемкость при постоянном объеме - соответствует процессу подвода тепла при постоянном объеме, когда не совершается работа расширения и количество тепла соответствует изменению внутренней энергии
![]() ; (3.2)
; (3.2)
· теплоемкость при постоянном давлении
![]() (3.3)
(3.3)
соответствует процессу подвода тепла при постоянном давлении, когда повышение температуры приводит к изменению объема и, таким образом, одновременно совершается некоторая работа расширения ![]() . Поскольку при изобарическом нагревании часть тепла помимо увеличения внутренней энергии идет на работу расширения, то
. Поскольку при изобарическом нагревании часть тепла помимо увеличения внутренней энергии идет на работу расширения, то ![]() .
.
Для идеального газа
![]() , (3.4)
, (3.4)
где R – газовая постоянная.
На величину теплоемкости влияет природа вещества. Так, газы со сходным строением молекул имеют близкие значения теплоемкостей. С усложнением строения молекул теплоемкость, как правило, возрастает. Повышение температуры также обычно приводит к росту теплоемкости. Температурную зависимость теплоемкости нельзя получить на основе законов термодинамики, ее определяют опытным путем. Зависимость теплоемкости от температуры имеет достаточно сложный вид, для описания ее в относительно узком интервале температур в большинстве случаев используют степенные уравнения вида
![]() (3.5)
(3.5)
или
![]() . (3.6)
. (3.6)
Значения коэффициентов этих уравнений для многих веществ можно найти в [6].
Влияние температуры на теплоемкость жидкости меньше, чем на теплоемкость газов. Теплоемкость твердых тел при низких температурах резко уменьшается и стремится к нулю при приближении температуры к абсолютному нулю.
Теплоемкость многоатомных газов, находящихся под небольшими давлениями, практически зависит только от температуры (у одноатомных, идеальных газов она постоянна). Теплоемкость реальных газов меняется и с температурой, и с давлением, причем с повышением температуры эффект воздействия давления уменьшается. Влияние давления велико вблизи кривой насыщения, в сверхкритической и особенно в критической области, так как в критической точке значение Cv проходит через максимум, а Cp стремится к бесконечности. Влиянием давления на теплоемкость твердых тел можно пренебречь. Теплоемкость жидкостей с давлением меняется незначительно; только вблизи кривой насыщения и более всего в критической области влияние давления становится существенным.
Экспериментальное определение теплоемкости обычно проводят при постоянном давлении, и потому в справочной литературе чаще приводятся значения Cр. В практике химических расчетов также чаще используются теплоемкости при постоянном давлении, поэтому в “Пособии” нами рассмотрены методы их прогнозирования. Ниже приведены методы прогнозирования теплоемкости при постоянном давлении, равном стандартному (1 физическая атмосфера) - ![]() .
.
Смотрите также
Миграция химических элементов
...
Аварийно химически опасные вещества
В соответствие с новым
ГОСТом, переименованы на АХОВ (аварийно химически опасные вещества) Понятия о
АХОВ Растет ассортимент применяемых в промышленности, сельском хозяйстве и быту
химическ ...
Проблемы государственного регулирования нефтяного комплекса России в условиях рынка
...
