Кислотность неводных растворов. Шкала рНрСтатьи / Стандартизация измерения рН в неводных средах. Методы определения рН стандартных буферных растворов / Кислотность неводных растворов. Шкала рНрСтраница 1
Важным вопросом является определение рН в неводных и смешанных растворителях. Этот вопрос имеет практическое значение, так как в пищевой промышленности, промышленности пластмасс, фото- кино- промышленности и других отраслях промышленности широко используют измерения рН в неводных растворах.
При определении рН в неводных растворах делается еще большее количество ошибок, чем при определении рН в водных растворах.
При решении проблемы о кислотностях неводных растворов следует поставить два вопроса. Как поступать при сравнении кислотности двух растворов в одном и том же растворителе? Как поступать при сравнении кислотности растворов в двух разных растворителях? Эта задача отличается принципиально от задачи сравнения между собой кислотности в пределах одного растворителя.
Очень часто намерении pН в неводных растворах производят по отношению к водному каломельному электроду, потенциал которого определяется по водному стандарту. При этом фактически измерения сводят к измерению э.д.с цепи:
Pt(H2) | стандартный | исследуемый | Pt(H2) (2.1.1)
р-р в воде р-р в неводн р-ле
Таким образом значения рН неводных растворов не могут быть получены путем непосредственного сопоставления потенциалов индикаторных электродов в водных и неводных растворах, а следовательно, и рН-метр, калиброванный по водным стандартам, не может дать правильных значений рН неводного раствора.
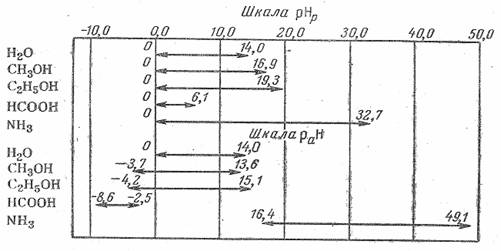
Рис. 1. Шкала рНр и шкала раН в различных растворителях.
По вопросу о стандартизации рН в неводных растворах нет единого мнения. Тем не менее расширение этого вопроса становится все более насущным в связи с широким распространением неводных растворителей, и особенно их смесей с водой, в промышленности и аналитической практике.
Задача сравнения кислотности в пределах одного неводного растворителя принципиально не отличается от задачи определения рН в водных растворах. Величина рН определяется отрицательным логарифмом активности ионов водорода в данном растворителе М:
pHp=-lga*=-lgc![]() *
*
т.е. отрицательным логарифмом произведения концентрации ионов лиония
на соответствующий концентрационный коэффициент активности. Коэффициент активности относится к бесконечно разбавленному раствору в данной среде как стандарту.
Переходя от воды в неводному растворителю, переходят от кислотности, выраженной в концентрациях или активностях одного иона - иона гидроксония, к кислотности, выраженном в концентрациях или активностях другого иона – лиония. Действительно, в воде носителем кислотных свойств является ион Н3О+. Когда по отношению к водному раствору мы говорим, что его рН = 5, это значит, что активность ионов Н3О+ равна 10-5. В спиртовом растворе носителем кислотных свойств являются ионы этоксония С2Н5ОН2+, в аммиаке носителем кислотных свойств — соответственно ионы аммония NH4+ и т. д.
При оценке рН растворов в пределах одного растворителя следует учитывать протяженность шкалы рН: в.воде вся шкала рН равна 14,0, но в этиловом спирте 19,3; в муравьиной кислоте. 6,1 и т. д. (рис. 1)
Стандартизация рН в неводных растворах может быть выполнена так же как и в водных растворах, т. е. путем изготовления стандартных растворов в том же растворителе, что и исследуемый раствор. Однако в этом случае возникает ряд затруднений. Например, коэффициенты активности сильных кислот значительно больше отличаются от единицы, чем в водных растворах; сильные в воде кислоты становятся в неводных растворах слабыми; хуже растворимы соли; значительно меньше имеется данных о коэффициентах активности.
В настоящее время единственным веществом, с помощью которого может быть произведена стандартизация рН в неводных растворах, является хлористый водород, так как для него имеются данные о коэффициентах активности в большинстве широко используемых растворителей и в их смесях с водой. В качестве электрода сравнения при измерениях в неводных растворах может быть использован хлорсеребрянный электрод в растворе НCl, который вполне пригоден для измерений в ряде чистых неводных растворителей и их смесях с водой.
Измеренная по отношению к стандарту в данном растворителю рН не является абсолютном мерой кислотности неводного раствора и может быть использована для характеристики кислотности только в пределах данного растворителя. Это следует из того, что начало шкалы кислотности раНр =0 не соответствует равенству абсолютных активностей ионов водорода во всех растворителях. Величины раН нейтральных растворов в разных растворителях не совпадают друг с другом, так как протяженность шкал, зависящая от ионного произведения растворителя, различна. В верхней части рис. 1 в качестве примера приведены шкалы рНр в воде и не которых неводных средах. В воде шкала рН изменяется от 0 до 14; нейтральным раствором называется раствор с рН = 7. Если раствор имеет рН=0, это раствор кислоты с активностью ионов Н+, равной единице; если раствор имеет рН = 14, это раствор щелочи с активностью ионов ОН--, равной единице, но это не значит, что не может быть растворов в воде с рН меньше нуля и больше 14.
Смотрите также
Введение
Свою дипломную работу хочу
начать со слов ученого-земляка М.В. Ломоносова, которые являются эпиграфом
данной работы:
“Вольность и союз наук необходимо
требуют взаимного сообщения и беззавистного ...
Германий (Germanium), Ge
Германий - химический элемент IV группы периодической системы Менделеева; порядковый номер 32, атомная масса 72,59; твёрдое вещество серо-белого цвета с металлическим блеском. Природный Г. представляе ...
