Физико-химические свойства системы, положенной в основу химико-технологического
процесса окисления сернистого ангидрида.Статьи / Производство серной кислоты / Физико-химические свойства системы, положенной в основу химико-технологического
процесса окисления сернистого ангидрида.Страница 2
η

Рис. 6. Зависимость выхода оксида серы (IV) от температуры при различном времени контактирования.
От скорости окисления зависит количество оксида серы (IV), окисляющееся в единицу времени, и, следовательно, объем контактной массы, размеры реактора и другие характеристики процесса. Организация этой стадии производства должна обеспечить возможно более высокую скорость окисления при максимальной степени контактирования, достижимой в данных условиях.
Энергия активации реакции окисления оксида серы (IV) кислородом в оксид серы (VI) весьма велика. Поэтому, в отсутствие катализатора реакция окисления даже при высокой температуре практически не идет. Применение катализатора позволяет снизить энергию активации и увеличить скорость окисления.
В производстве серной кислоты в качестве катализатора применяют контактные массы на основе оксида ванадия (V) марок БАВ и СВД, названные так по начальным буквам элементов, входящих в их состав.
БАВ (барий, алюминий, ванадий) состава:
V2О5 (7 %) + К2SО4 + ВаSО4 + Аl2(SО4)3 + SiО2 (кремнезем)
![]()
катализатор активатор носитель
СВД (сульфо–ванадато–диатомовый) состава
V2О5 (7 %) + К2S2О7 + диатомит + гипс
![]()
катализатор активатор носитель
Для описания скорости окисления оксида серы (IV) в оксид серы (VI) на ванадиевом катализаторе при неподвижном слое катализатора предложены различные кинетические уравнения. К ним относится, например, уравнение (4), связывающее скорость реакции со степенью превращения оксида серы (IV), константой скорости реакции , константой равновесия и давлением газа:
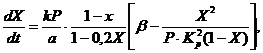 (4)
(4)
![]() (5)
(5)
где Х – равновесная степень превращения оксида серы (IV),
k – константа скорости окисления,
а – начальная концентрация оксида серы (IV) в газе,
b – начальная концентрация кислорода в газе,
Р – общее давление в газе,
Кр – константа равновесия реакции.
Из уравнений (4) и (5) следует, что скорость окисления зависит от константы скорости реакции, сильно возрастающей при повышении температуры. Однако при этом уменьшается константа равновесия Кр и уменьшается значение члена 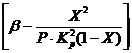 в уравнении (4). Таким образом, скорость процесса окисления оксида серы (IV) зависит от двух величин, изменяющихся с ростом температур в противоположном направлении. Вследствие этого кривая зависимости скорости окисления от температуры должна проходить через максимум. Из уравнения (4) также следует, что скорость окисления оксида серы (IV) тем больше, чем меньше достигаемая в этом процессе степень превращения оксида серы (IV) в оксид серы (VI). Вследствие этого для каждой степени превращения зависимость скорости реакции от температуры будет выражаться индивидуальной кривой, имеющей максимум. На рис. 7 представлена серия подобных кривых, соответствующих различные степеням превращения для газа постоянного состава. Из него следует, что скорость реакции окисления достигает максимума при определенных значениях температур, которая тем выше, чем меньше эта степень превращения, и представляют, очевидно, оптимальные температуры.
в уравнении (4). Таким образом, скорость процесса окисления оксида серы (IV) зависит от двух величин, изменяющихся с ростом температур в противоположном направлении. Вследствие этого кривая зависимости скорости окисления от температуры должна проходить через максимум. Из уравнения (4) также следует, что скорость окисления оксида серы (IV) тем больше, чем меньше достигаемая в этом процессе степень превращения оксида серы (IV) в оксид серы (VI). Вследствие этого для каждой степени превращения зависимость скорости реакции от температуры будет выражаться индивидуальной кривой, имеющей максимум. На рис. 7 представлена серия подобных кривых, соответствующих различные степеням превращения для газа постоянного состава. Из него следует, что скорость реакции окисления достигает максимума при определенных значениях температур, которая тем выше, чем меньше эта степень превращения, и представляют, очевидно, оптимальные температуры.

Рис. 7. Зависимость скорости окисления оксида серы (IV) от температуры при различных степенях превращения Х1 < Х2 < Х3 < Х4
Линия АА, соединяющая точки оптимальных температур, называется линией оптимальной температурной последовательности (ЛОТ) и указывает, что для достижения наилучших результатов процесс контактирования следует начинать при высокой температуре, обеспечивающей большую скорость процесса (на практике около 600 оС), а затем для достижения высокой степени превращения снижать температуру, выдерживая температурный режим по ЛОТ. Линии ВВ и СС на рис. 7 очерчивают область допустимых температур в реальном технологическом процессе контактирования.
В таблице 2 представлен температурный режим работы 4-х слойного контактного аппарата с промежуточным теплообменом, установленный в соответствии с изложенным выше принципом:
Таблица 2. Температурный режим контактного узла
|
Слои |
I |
II |
III |
IV |
|
Температурный режим в контактном аппарате, оС |
440–600 |
460–500 |
440–450 |
420–425 |
|
Температурный режим в теплообменнике, оС |
600–460 |
500–440 |
450–420 |
420 |
|
Хр |
0,70 |
0,90 |
0,96 |
0,98 |
Смотрите также
Химический анализ катионов
Основой любого химического
исследования является совокупность различных химических наук, каждая из которых
нуждается в результатах химического анализа, поскольку химический состав –
основа ...
