Описание технологического процессаСтатьи / Производство кальцинированной соды / Описание технологического процессаСтраница 2
![]() CaO+ H2O→ Ca(OH)2 –ΔΗ=63,8 кДж/моль
CaO+ H2O→ Ca(OH)2 –ΔΗ=63,8 кДж/моль
![]() Ca(OH)2 +2 NH4Cl→2 NH3 + CaCl2 + H2O+ΔΗ=27,6
Ca(OH)2 +2 NH4Cl→2 NH3 + CaCl2 + H2O+ΔΗ=27,6
NaHCO3→Na2CO3+ CO2+ H2O+ΔΗ
Реализация химической модели сопряжена с разработкой технологического режима с использованием физико – химических свойств водной четырехкомпонентной системы.
В водном растворе существуют четыре компонента NaCl – NH4HCO3 - NH4Cl – NaHCO3 (независимых компонентов – четыре, ибо если известны значения трех компонентов, то по уравнению реакции можно рассчитать содержание четвертого.) Соль NH4HCO3 образуется в результате взаимодействия в растворе СО2 и NH3:
СО2 (p) + 2NH3(p)↔NH2COONH4(p) – ΔΗ1
Образовавшийся карбамат гидролизуется:
NH2COONH4(p) + H2O ↔ NH4HCO3(р) + NH3(p) + ΔΗ2 - ΔΗ + ΔΗ= -63,8 кДж
Температурный режим избран по результатам исследования реакций, а материальные расчеты и соотношения реагирующих компонентов определены по данным о четырехполюсной системе. Ниже приведены графические методы разработки технологического режима для реакций такого типа. На основании диаграммы (рис.1) устанавливают, что хлорид натрия взаимодействует с бикарбонатом аммония, образуя бикарбонат натрия и хлорид аммония, и растворимость бикарбоната натрия в этой системе мала, так как в равновесном растворе 1 моль бикарбоната растворяется в 4240 молях воды, т.е. практически впадает в твердую фазу. Проекция диаграммы на квадрат солевого состава представлена на рис.2
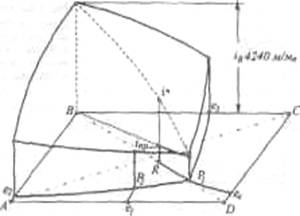
Рис. 3. Система Na+, NH+4║Cl-, HCO3- - H2O, Т 30ºС: А-NaС1; B-NaHCO3; C-NH4HCO3; D - NH4C1; i-количество Н2О - молей воды/1 моль Σ солей; i* -равновесное, inp - практическое R-отношение А : С, вступающих в реакцию; Р – солевой состав раствора
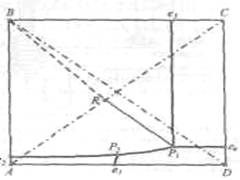
Рис.4. Проекция системы Na+, NH4+║Cl-, HCO-3- H2O, Т 30ºС: А-NaС1; B-NaHCO3; C-NH4HCO3; D - NH4C1; e – солевой состав эвтонических растворов двухкомпонентных систем; Р – нонвариантные точки четырех - компонентной системы; R – солевой состав реакционной смеси
Стабильной диагональю солевого квадрата, которая пересекает только два полюса кристаллизации, является диагональ бикарбоната натрия – хлорид аммония, соотношение между реагирующими компонентами выбирают графически по проекции диаграммы, учитывая необходимость получения бикарбоната натрия, не содержащего в твердой фазе аммонийных солей. Иллюстрацией этого приема служит рис 3. Он заключается в создании в растворе несколько увеличенного содержания воды по сравнению с нонвариантной фигуративной точкой Р1, на которую направлен луч кристаллизации.
Смотрите также
Поведение полимерных веществ в присутствии ионов металлов
Исследование поведения полимеров (в том числе полимерных гидрогелей) в
растворах солей металлов представляет собой огромный практический и
теоретический интерес. Изучение особенностей тако ...
Получение диметилового эфира дегидратацией метанола на АlPO4 +SiO2 катализаторах
...
Извлечение серебра из отработанных фотографических растворов
В процессе
фиксации фотографической пленки для удаления невосстановившегося серебра с
пленки применяют тиосульфат натрия или аналогичные реактивы, например
тиосульфат калия, тиосульфат аммо ...
