Энергетические уровни жесткого ротатора и его спектрСтатьи / Полярные диаграммы и энергетические уровни волновых функций жесткого ротатора / Энергетические уровни жесткого ротатора и его спектр
Поскольку квадрат момента импульса в жестком ротаторе однозначно связан с энергией (4.47), формула (4.101) позволяет легко рассчитать его уровни и спектральные термы (Т
), т.е. уровни, выраженные в единицах измерения волнового числа (см–1 ) , являющегося характеристикой излучения
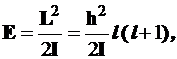 (4.105)
(4.105)
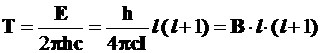 . (4.105)
. (4.105)
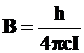 (4.107)
(4.107)
Величина В, определяемая (4.107), называется вращательной постоянной ротатора.
4.3.7.2. Обозначим величину 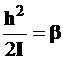 и составим таблицу 4.5 возможных значений энергии жесткого ротатора, а на рис. 4.5. представим его энергетическую диаграмму.
и составим таблицу 4.5 возможных значений энергии жесткого ротатора, а на рис. 4.5. представим его энергетическую диаграмму.
4.3.7.3. Подобно плоскому ротатору, энергетическая диаграмма жесткого ротатора демонстрирует расходящуюся систему уровней, однако значительно возрастает кратность вырождения. Расстояния между соседними уровнями увеличиваются с ростом квантового числа l, причем они линейно связаны с квантовым числом нижнего уровня l:
![]() . (4.108)
. (4.108)
Таблица 4.5.
Уровни жесткого ротатора
|
l |
Символ уровня |
Энергия Е, |
Вырождение g=2l+1 |
|
0 |
S |
0 |
1 |
|
1 |
P |
2 |
3 |
|
2 |
D |
6 |
5 |
|
3 |
F |
12 |
7 |
|
4 |
G |
20 |
9 |
Рис. 4.5. Энергетическая диаграмма жесткого ротатора.
Для жесткого ротатора, например, двухатомной молекулы, разрешены спектральные переходы между соседними уровнями ![]() . Поэтому, согласно уравнению 4.108, ее спектр представляет собой набор линий, отстоящих друг от друга на примерно одинаковую величину, равную
. Поэтому, согласно уравнению 4.108, ее спектр представляет собой набор линий, отстоящих друг от друга на примерно одинаковую величину, равную ![]() в энергетической шкале, или 2В в шкале волновых чисел
в энергетической шкале, или 2В в шкале волновых чисел ![]() .
.
Поскольку вращательная постоянная связана с моментом инерции, изучение вращательных спектров молекул даёт возможность экспериментального определения момента инерции молекул и, следовательно, межатомных расстояний.
Смотрите также
Коррозия металлов и методы защиты от неё
...
Стеклокристаллические материлы (ситаллы)
...
Бром (Bromum), Br
Бром - химический элемент VII группы периодической системы Менделеева, относится к галогенам; атомный номер 35, атомная масса 79,904; красно-бурая жидкость с сильным неприятным запахом. Б. откры ...
