Рибонуклеозиды (на примере инозина)Статьи / Полупрепаративный микробиологический синтез биологически активных соединений, меченных стабильными изотопами водорода и углерода / Рибонуклеозиды (на примере инозина)
2
Н-меченый инозин.
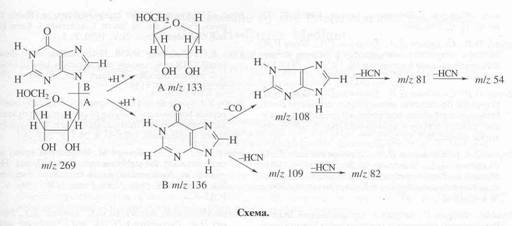
Уровень дейтерированности определяли методом масс-спектрометрии FAB. Фрагментация молекулы инозина при бомбардировании быстрыми электронами заключается в формировании ионизированного пика его молекулярного иона [М + Н]+ при m/z 269, который впоследствии распадается на фрагмент рибозы А при m/z 133 и гипоксантиновый фрагмент В при m/z 136, расщепляющийся в свою очередь на ряд менее низкомолекулярных осколочных фрагментов при m/z 54, ., 109 за счет элиминирования НСN и СО из гипоксантина (схема). Уровень дейтерированности инозина составил пять атомов из восьми детектируемых по скелету молекулы или 62.5% относительно общего количества атомов водорода в углеродном скелете молекулы. Примеси молекул с включением четырех (m/z при 273, 23%), шести (m/z при 275, 32%) и семи атомов дейтерия (m/z при 276, 20%) также фиксировались в масс-спектре (рис. 19). Возможные места локализации дейтерия определяли по тяжелым пикам фрагментов рибозы C5H9O4+ при m/z 136, 46% (вместо m/z 133, 42%) и гипоксантина C5H4ON4+ при m/z 138, 54% (вместо m/z 136, 50%) в масс-спектре. Исходя из полученных данных можно предположить, что три атома дейтерия локализуются в рибозной части молекулы и два - в гипоксантиновом остатке. Достоверность полученного результата подтверждалась присутствием тяжелых пиков низкомолекулярных фрагментов, продуктов распада гипоксантина при m/z 84, 42% (вместо m/z при 82, 40%), и 111, 49% (вместо m/z при 109, 45%).
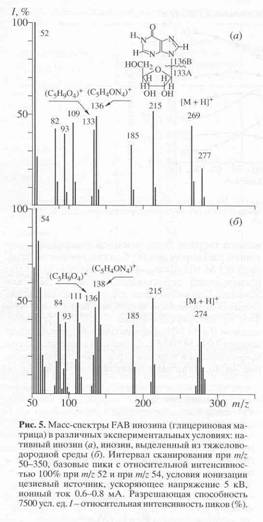
При анализе уровня дейтерированности 2Н-меченого инозина руководствовались следующими аспектами. Во-первых, изотопный полиморфизм свидетельствует о низкой специфичности изотопного включения дейтерия в молекулу инозина и, по-видимому, определяется условиями самого биосинтеза. Во-вторых, вследствие того что протоны (дейтероны) в С’1-С’5 положениях рибозной части могли происходить из глюкозы, предпологалось, что биосинтетическое включение дейтерия в рибозную часть молекулы инозина определяется в основном функционированием ряда процессов ГМФ-шунта, связанных непосредственно с ассимиляцией глюкозы. Вследствие того что глюкоза использовалась в протонированном виде, ее вклад в уровень дейтерированности рибозного фрагмента пренебрегался. Однако, вопреки этому предположению наблюдалось включение дейтерия в рибозный фрагмент молекулы инозина, что могло быть следствием сохранения доли минорных путей биосинтеза глюкозы из предшественников de novo. В-третьих, возможные (Н - 2Н) обменные процессы и изомеризационные превращения, происходящие во внутриклеточной среде в присутствии 2Н2O могли приводить к специфическому включению дейтерия по определенным позициям в молекуле инозина. Такими доступными позициями в молекуле инозина признаны прежде всего протоны при гидроксильных группах -ОН в рибозном остатке и имидазольные протоны при гетероатомах -NH (последние могут обмениваться на дейтерий в 2Н2O за счет кето-енольной таутомерии). Атомы дейтерия в остатке гипоксантина включались из 2Н-меченых аминокислот.
Смотрите также
Введение
В условиях развития современного общества
повышаются требования к качеству обучения школьников, уровню знаний и умений
учащихся. При том, резко возрастает нагрузка на весь образовательный процесс в
...
Классификация дисперсных систем по агрегатному состоянию. Особенности каждой системы
...
Поведение полимерных веществ в присутствии ионов металлов
Исследование поведения полимеров (в том числе полимерных гидрогелей) в
растворах солей металлов представляет собой огромный практический и
теоретический интерес. Изучение особенностей тако ...
