Химическое равновесиеПериодическая система / Методика решения задач по теоретическим основам химической технологии / Химическое равновесиеСтраница 1
При протекании химической реакции через некоторое время устанавливается равновесное состояние (химическое равновесие). Слово «равновесие» означает состояние, в котором сбалансированы все противоположно направленные на систему воздействия. Тело, находящееся в состоянии устойчивого равновесия, обнаруживает способность возвращаться в это состояние после какого-либо возмущающего воздействия.
Примером тела, находящегося в состоянии устойчивого равновесия, может служить шарик, лежащий на дне ямки. Если его толкнуть в одну или другую сторону, он вскоре снова возвращается в состояние устойчивого равновесия. В отличие от этого шарик, лежащий на краю ямки, находится в состоянии неустойчивого равновесия — достаточно ничтожного толчка, чтобы он необратимо скатился в ямку.
Оба этих примера являются примерами статического равновесия. В химии, однако, приходится сталкиваться не столько со статическими равновесиями, столько с динамическими («подвижными»). Динамическое равновесие устанавливается, когда оказываются сбалансированными два обратимых или противоположных процесса. Динамические равновесия подразделяют на физические и химические. Наиболее важными типами физических равновесий являются фазовые равновесия. Система находится в состоянии химического равновесия, если скорость прямой реакции равна скорости обратной реакции.
Например, если скорость протекания реакции (константа скорости к1)
k1
А(г) + В(пар) ![]() АВ(г)
АВ(г)
равна скорости обратной реакции (константа скорости k2)
k2
АВ(г)![]() А(г) + В(пар)
А(г) + В(пар)
то система находится в динамическом равновесии. Подобные реакции называются обратимыми, а их уравнения записывают с помощью двойной стрелки:
k1
А(г) + В(пар) ![]() АВ(г)
АВ(г)
k2
Реакции, протекающие слева направо, называются прямой, справа налево – обратной.
Нужно подчеркнуть, что реакционная система остается в состоянии динамического равновесия лишь до тех пор, пока система остается изолированной. Изолированной называют такую систему, которая не обменивается с окружающей средой ни веществом, ни энергией.
Состояние химического равновесия обратимых процессов количественно характеризуется константой равновесия. Так, для обратимой реакции общего вида
k1
аA +bB ![]() сC + dD (1.2.1)
сC + dD (1.2.1)
k2
константа равновесия К
, представляющая собой отношение констант скорости прямой и обратной реакций, запишется
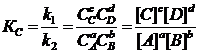 (1.2.2)
(1.2.2)
где, Кс– константа скорости реакции, зависящая от концентрации реагирующих компонентов; Сi
или [ i ]-
равновесная молярная концентрация i-того компонента;
a, b, c, d
– стехиометрические коэффициенты веществ.
В правой части уравнения (1.2.2) стоят концентрации взаимодействующих частиц, которые устанавливают при равновесии, - равновесные концентрации.
Уравнение (1.2.2) представляет собой математическое выражение закона действующих масс при химическом равновесии. Для реакции с участием газов константа равновесия выражается через парциальные давления, а не через их равновесные концентрации. В этом случае константу равновесия обозначают символом Кр.
![]()
Рi
- равновесные парциальные давления i-того компонента.
Сi
- равновесная молярная концентрация компонентов.
a, b, c, d
–
стехиометрические коэффициенты веществ.
Состояние химического равновесия при неименных внешних условиях теоретически может сохраняться бесконечно долго. В реальной действительности, т.е. при изменении температуры, давления или концентрации реагентов, равновесии может «сместиться» в ту или иную сторону протекания процесса.
Изменения, происходящие в системе в результате внешних воздействий, определяется принципом подвижного равновесия – принципом Ле Шателье – Брауна. При воздействие на равновесную систему, любого внешнего фактора, равновесие в системе смещается в таком направлении, чтобы уменьшить воздействие этого фактора.
1.
Влияние давления на равновесие химической реакции (для реакции, проходящей в газовой фазе).
Смотрите также
Металлы
...
Соединения азота
Анализ содержания экспериментальной части программы
по данной теме свидетельствует, что большинство продуктов реакций являются
минеральными удобрениями. Утилизировать отходы можно по следующ ...
Современные направления развития композитов на основе полимеров
Современная техника предъявляет самые
разнообразные требования к полимерным материалам. Допустим, нужно повысить
прочность и жесткость полимера, снизить его стоимость, уменьшить плотность. С ...
